
四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍; D是形成化合物种类最多的元素.
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为 5:1 ;写出由甲制高聚物的反应方程式 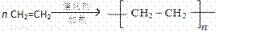 .
.
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于 (“极性分子”或“非极性分子”);其电子式 ;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式.
(3)写出B的基态原子电子排布图为  .与PH3相比,DC2易液化的主要原因是 ;
.与PH3相比,DC2易液化的主要原因是 ;
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与CO2分子具有相似的结构.故B2C的空间构型是 ,其为 (填“极性”或“非极性”)分子.
考点:
位置结构性质的相互关系应用.
分析:
四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子,则A为H;B的基态原子s能级的总电子数比p能级的总电子数多1,电子排布为1s22s22p3,则B为N;C元素的原子最外层电子数是次外层的3倍,则应为2个电子层,最外层电子数为6,即C为O; D是形成化合物种类最多的元素,D为C元素,以此来解答.
解答:
解:依据分析可知A为氢、B为氮、C为氧、D为碳,
(1)A、D形成的化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,故甲为乙烯,分子式为C2H4,含4个C﹣H和1个C=C键,则σ键和π键数目之比为5:1;乙烯加聚生成聚乙烯,化学反应方程式为: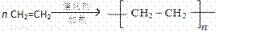 ,故答案为:5:1;
,故答案为:5:1;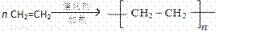 ;
;
(2)A、C形成的化合物A2C2分子的电子式为 ,属于极性分子,故答案为:极性分子;
,属于极性分子,故答案为:极性分子;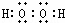 ;
;
(3)B的基态原子电子排布图为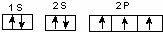 ;与PH3相比,BA3易液化,是因氨气分子之间存在氢键,沸点高易液化,故答案为:
;与PH3相比,BA3易液化,是因氨气分子之间存在氢键,沸点高易液化,故答案为: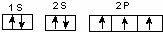 ;氨气分子之间存在氢键;
;氨气分子之间存在氢键;
(4)N2O与CO2具有相似的结构,应为直线形分子,且存在N=O键,N2O分子中氧原子只与一个氮原子相连,应为N=N=O结构,氮和氮原子之间的化学键是非极性共价键,故答案为:直线型,非极性.
点评:
本题考查位置、结构、性质的关系及应用,为高频考点,把握原子结构、电子排布推断元素为解答的关键,侧重物质结构与性质的考查及分析、推断能力的考查,题目难度不大.


科目:高中化学 来源: 题型:
同温同压下,某容器充满O2重116g,若充满CO2重122g,现充满某气体重124g,则某气体的相对分子质量为( )
|
| A. | 4 | B. | 28 | C. | 32 | D. | 48 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,把铁片和锌片放在盛有稀食盐水和酚酞溶液的混合液中,此装置中锌片是 极,电极反应式为 ;铁片是 极,电极反应式为 ;电解质溶液在 片周围的溶液先呈红色.

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中错误的是( )
|
| A. | SO2、SO3都是极性分子 |
|
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 |
|
| C. | 元素电负性越大的原子,吸引电子的能力越强 |
|
| D. | PCl3和NF3分子中所有原子的最外层都达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程中化学键被破坏的是( )
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水⑤MgCl2溶解于水 ⑥NaCl熔化.
|
| A. | 全部 | B. | ②③④⑤⑥ | C. | ④⑤⑥ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子中,能在溶液中大量共存的是( )
|
| A. | H+ Na+CO32﹣ Cl﹣ | B. | Ba2+ Na+Cl﹣ SO42﹣ |
|
| C. | K+ H+ SO42﹣OH﹣ | D. | Ag+ Al3+ NO3﹣H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各关系式中能说明反应N2+3H2⇌2NH3已达到平衡状态的是( )
|
| A. | 3υ正(N2)=υ正(H2) | B. | υ正(N2)=υ逆(NH3) |
|
| C. | υ正(N2)=3υ逆(H2) | D. | 2υ正(H2)=3υ逆(NH3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com