
| 250 |
| 25 |
| 1.01×10-2mol×56g/mol |
| 5.40g |


科目:高中化学 来源: 题型:
| A、锌和硫酸反应:Zn+H2SO4=ZnSO4+H2 |
| B、碳酸钙和盐酸反应:CaCO3+2HCl=CaCl2+CO2+H2O |
| C、过氧化钠和水反应:2Na2O2+2H2O=4NaOH+O2 |
| D、铁和硫酸铜溶液反应:Fe+CuSO4=FeSO4+Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 称量氢氧化钠固体 |
B、 检验铁粉与水蒸气反应产生的氢气 |
C、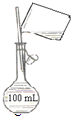 配制150mL 0.10 mol?L-1盐酸 |
D、 分离两种沸点相差较大的液体互溶混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH(开始沉淀) | 2.3 | 7.5 | 5.6 |
| pH(完全沉淀) | 3.9 | 9.7 | 6.4 |
2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸钠在水中电离:Na2SO4=Na++SO42- | ||||
B、二氧化锰和浓盐酸共热制氯气的离子方程式:MnO2+4H++4Cl-
| ||||
| C、甲烷燃烧的热化学方程式:CH4+202=CO2+2H2O△H═-889.6kJ?mol-1 | ||||
D、乙烯与水在催化剂、加热条件下反应:CH2═CH2+H2O
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com