
 ��
�� ��E��H��Ӧ����I�ķ���ʽΪ
��E��H��Ӧ����I�ķ���ʽΪ ��
��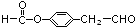 ��
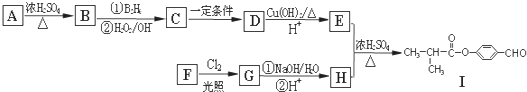
�� ���� AΪ�����Һ˴Ź���������2�ֲ�ͬ��ѧ�������⣬��AΪ��CH3��3COH��A��Ũ���ᡢ���������·�����ȥ��Ӧ����BΪCH2=C��CH3��2��B������Ϣ2�еķ�Ӧ����CΪ��CH3��2CHCH2OH��C��Cu��Ag�����������·�������������DΪ��CH3��2CHCHO��D����������ͭ��Ӧ������������Ӧ�����ữ�õ�EΪ��CH3��2CHCOOH����I�Ľṹ��֪��HΪ �����ƿ�֪GΪ
�����ƿ�֪GΪ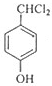 ��FΪ
��FΪ ������F�ķ���ʽΪC7H8O�������ϵ�һ�ȴ���ֻ�����ֵ�������F����ȡ����Ӧ����G��G����ˮ�⣬����ȡ����Ӧ����H���ݴ˽��
������F�ķ���ʽΪC7H8O�������ϵ�һ�ȴ���ֻ�����ֵ�������F����ȡ����Ӧ����G��G����ˮ�⣬����ȡ����Ӧ����H���ݴ˽��
��� �⣺AΪ�����Һ˴Ź���������2�ֲ�ͬ��ѧ�������⣬��AΪ��CH3��3COH��A��Ũ���ᡢ���������·�����ȥ��Ӧ����BΪCH2=C��CH3��2��B������Ϣ2�еķ�Ӧ����CΪ��CH3��2CHCH2OH��C��Cu��Ag�����������·�������������DΪ��CH3��2CHCHO��D����������ͭ��Ӧ������������Ӧ�����ữ�õ�EΪ��CH3��2CHCOOH����I�Ľṹ��֪��HΪ �����ƿ�֪GΪ
�����ƿ�֪GΪ ��FΪ
��FΪ ������F�ķ���ʽΪC7H8O�������ϵ�һ�ȴ���ֻ�����ֵ�������F����ȡ����Ӧ����G��G����ˮ�⣬����ȡ����Ӧ����H��
������F�ķ���ʽΪC7H8O�������ϵ�һ�ȴ���ֻ�����ֵ�������F����ȡ����Ӧ����G��G����ˮ�⣬����ȡ����Ӧ����H��
��1��BΪCH2=C��CH3��2��B�ķ���ʽΪC4H8��
�ʴ�Ϊ��C4H8��
��2����������ķ�����֪��C��DΪ������Ӧ��
�ʴ�Ϊ��������Ӧ��
��3��������������֪��F�Ľṹ��ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��4��D����E�Ļ�ѧ����ʽΪ�� ��E��H��Ӧ����I�ķ���ʽΪ��
��E��H��Ӧ����I�ķ���ʽΪ��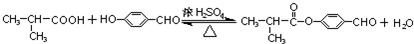 ��
��
�ʴ�Ϊ�� ��
�� ��
��
��5��I�� ����ͬϵ��K��I��Է�������С28����K��I��2��-CH2-ԭ���ţ�K�Ľṹ����ͬʱ���������������ٱ�����ֻ������ȡ�������ڷ����в�������
����ͬϵ��K��I��Է�������С28����K��I��2��-CH2-ԭ���ţ�K�Ľṹ����ͬʱ���������������ٱ�����ֻ������ȡ�������ڷ����в�������
����Ϊ-CHO��-CH2OOCH��-CH2CHO��-OOCH���ֽṹ�������ڡ��䡢������λ�ã�����6�֣�����ͬ���칹��������һ������NaOH�����л���ṹ��ʽΪ��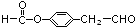 �ȣ�
�ȣ�
�ʴ�Ϊ��6��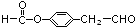 �ȣ�
�ȣ�
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶϼ�֪ʶǨ�����������ݷ�Ӧ�����������Ϣ������Ľṹ��ʽ�����ƶϣ���ȷ�ƶ����ʽṹ��ʽ�ǽⱾ��ؼ����ѵ��ǣ�5����ͬ���칹�������жϣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
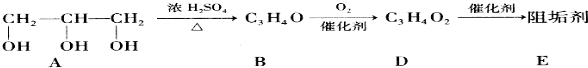
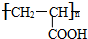 ���䷴Ӧ����Ϊ�Ӿ۷�Ӧ��
���䷴Ӧ����Ϊ�Ӿ۷�Ӧ��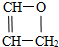 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
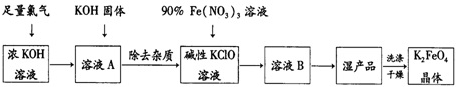
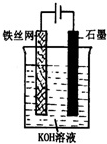
 �й�����ս����-31ʹ���˸�ǿ�ȡ����µ��ѺϽ���ϣ���ҵ��ұ���ѵķ�Ӧ���£�
�й�����ս����-31ʹ���˸�ǿ�ȡ����µ��ѺϽ���ϣ���ҵ��ұ���ѵķ�Ӧ���£�| A�� | TiCl4�ǻ�ԭ�� | B�� | Mg������ | ||
| C�� | TiCl4����������Ӧ | D�� | Mg�õ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼��������Һ�������ı���ʯ��ˮ��Ӧ2HCO3-+Ca2++2OH-�TCaCO3��+CO32-+2H2O | |
| B�� | ������������Һ�м���ϡ���ᡡOH-+H+�TH2O | |
| C�� | ���Ȼ�����Һ�м������ۡ�Fe+FeCl3=2Fe2++3Cl- | |
| D�� | Ca��ClO��2��Һ��ͨ������Ķ�����������Ca2++2ClO-+H2O+SO2�TCaSO3��+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NO | B�� | O3 | C�� | CO2 | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��10mL��Ͳ��ȡϡ������Һ 8.0mL | |
| B�� | �ø����pH��ֽ�ⶨ��ˮ��pH | |
| C�� | �ü�ʽ�ζ�����ȡKMnO4��Һ 19.60mL | |
| D�� | ʹ������ƿ������Һʱ������Һ�涨�ݺ�������Һ��Ũ��ƫ�� | |
| E�� | Բ����ƿ����ƿ�����������ʱ��Ӧ����ʯ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com