
分析 (1)实验室制乙烯时,温度计测量溶液温度;而石油分馏时,温度计测量馏分温度;
(2)卤代烃中检验溴元素时,卤代烃发生水解反应或消去反应后,在滴加硝酸银溶液之前应该滴加稀硝酸溶液;
(3)Ag和稀硝酸反应生成可溶性的硝酸银;
(4)淀粉用碘检验;
(5)银氨溶液的配制:向硝酸银溶液中滴加氨水(边滴加边摇动)至产生的沉淀恰好溶解即可;
(6)己烯和溴发生加成反应而使溴水褪色,苯酚和溴水反应生成白色沉淀,甲苯和乙酸乙酯都不和溴水反应,甲苯能被酸性高锰酸钾溶液氧化,乙酸乙酯和酸性高锰酸钾溶液不反应.
解答 解:(1)实验室制乙烯时,温度计测量溶液温度,所以温度计水银球插入溶液中;而石油分馏时,温度计测量馏分温度,所以温度计水银球位于蒸馏烧瓶支管口处,故正确;
(2)卤代烃中检验溴元素时,卤代烃发生水解反应或消去反应后,在滴加硝酸银溶液之前应该滴加稀硝酸溶液,防止生成AgOH造成干扰,故错误;
(3)Ag和稀硝酸反应生成可溶性的硝酸银,所以做过银镜反应的试管用稀硝酸洗涤,故正确;
(4)淀粉用碘检验,所以用碘检验淀粉,故错误;
(5)银氨溶液的配制:向硝酸银溶液中滴加氨水(边滴加边摇动)至产生的沉淀恰好溶解即可,注意不能将硝酸银溶液滴入氨水中,故正确;
(6)己烯和溴发生加成反应而使溴水褪色,苯酚和溴水反应生成白色沉淀,甲苯和乙酸乙酯都不和溴水反应,甲苯能被酸性高锰酸钾溶液氧化,乙酸乙酯和酸性高锰酸钾溶液不反应,反应现象不同,所以可以用溴水、高锰酸钾溶液鉴别己烯、甲苯、乙酸乙酯、苯酚溶液,
故答案为:(1)、(3)、(5)、(6).
点评 本题考查化学实验方案评价,为高频考点,涉及物质鉴别、溶液配制、物质检验、仪器使用等知识点,根据物质的性质及性质差异性选取检验试剂,注意银氨溶液配制方法,易错题是(2)题.


科目:高中化学 来源: 题型:选择题
| A. | 原子核外电子的每一个能层最多可容纳的电子数为2n2 | |
| B. | 任一能层的能级总是从s能级开始,而且能级数不一定等于该能层序数 | |
| C. | 同是s能级,在不同的能层中所能容纳的最多电子数是不相同的 | |
| D. | 1个原子轨道里最多只能容纳2个电子,但自旋方向相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
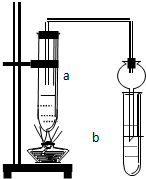 如图所示,在试管a中先加2mL乙醇,边摇动边缓缓加入5mL浓硫酸,摇匀冷却后,再加入2g无水醋酸钠,充分搅动后,固定在铁架台上.在试管b中加入适量的饱和Na2CO3溶液.连接好装置,给a加热,当观察到试管b中有明显现象时,停止实验.
如图所示,在试管a中先加2mL乙醇,边摇动边缓缓加入5mL浓硫酸,摇匀冷却后,再加入2g无水醋酸钠,充分搅动后,固定在铁架台上.在试管b中加入适量的饱和Na2CO3溶液.连接好装置,给a加热,当观察到试管b中有明显现象时,停止实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.089 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2、+4、+6 | +3 | -2 |
| A. | 单质与稀硫酸反应的速率快慢:R>Y>X | |
| B. | 离子半径:X2+>T2- | |
| C. | 元素最高价氧化物对应的水化物的碱性:R>X | |
| D. | 相同条件下,等物质的量的单质与氢气化合放出能量的多少:T>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; 业生产中M与水反应的产物之一可用于漂泊和杀菌,写出M与水初步反应的化学方程式NCl3+3H2O═NH3+3HClO.
业生产中M与水反应的产物之一可用于漂泊和杀菌,写出M与水初步反应的化学方程式NCl3+3H2O═NH3+3HClO.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl沉淀多于AgBr沉淀 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | 只有AgBr沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com