
【题目】(14分)
砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2O3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的学%科网关系如图所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的学%科网关系如图所示。
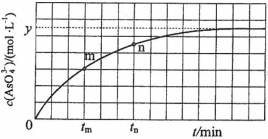
①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再变化
d. c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
【答案】
(1)![]()
(2)2As2S3+5O2+6H2O=4H3AsO4+6S 增加反应物O2的浓度,能够有效提高As2S3的转化率
(3)2△H1-3△H2-△H3
(4)①ac、大于、 小于、 tm时AsO43-浓度更小,反应速率更慢、K=![]()
【解析】
(1)砷是33号元素,原子核外电子排布式[Ar]3d104s24p3,原子结构示意图正确答案:![]() ;
;
(2)原已知可以得到As2S3+O2→H3AsO4+S,As2S3总共升高10价,得失电子配平得2As2S3+5O2→4H3AsO4+6S,再考虑质量守恒,反应前少12H、6O ,所以反应原理为2As2S3+5O2+6H2O=4H3AsO4+6S。该反应加压时,增加反应物O2的浓度,平衡正向移动,能够有效提高As2S3的转化率;
(3)待求解反应可以由反应①×2-反应②×3-反应③,则△H=2△H1-3△H2-△H3 ;
(4)①a溶液pH不变时,则c(OH-)也保持不变,反应处于平衡状态;b 根据速率关系,v(I-)/2=v(AsO33-),则b的等式始终成立,反应不一定处于平衡状态;c由于提供的Na3ASO3总量一定,所以c(AsO43-)/c(AsO33-)不再变化时,c(AsO43-)与c(AsO33-)也保持不变,反应处于平衡状态;d c(I-)=y mol/L时,从图中可以看出,反应处于平衡状态。正确答案:ACD。②反应从正反应开始进行,tm时反应继续正向进行,v正>v逆。正确答案:大于。③tm时比tn时AsO43-浓度更小,所以逆反应速率也更小,正确答案:小于、tm时AsO43浓度更小,反应速率更慢。④反应前,三种溶液混合后,Na3ASO3浓度为![]() ,同理I2浓度为xmol/L,反应达到平衡时,生成c(AsO43-)为ymol/L,则反应生成I-浓度c(I-)=2ymol/L,消耗AsO33-、I2浓度均为ymol/L,平衡时c(AsO33-)为 (x-y) mol/L,c(I2)为(x-y)mol/L,溶液中c(OH-)=1mol/L,K=
,同理I2浓度为xmol/L,反应达到平衡时,生成c(AsO43-)为ymol/L,则反应生成I-浓度c(I-)=2ymol/L,消耗AsO33-、I2浓度均为ymol/L,平衡时c(AsO33-)为 (x-y) mol/L,c(I2)为(x-y)mol/L,溶液中c(OH-)=1mol/L,K=![]() 。
。


科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础](15分)
化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:
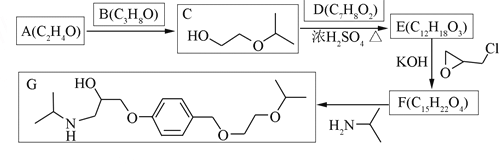
已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1molD可与1mol NaOH或2mol Na反应。
回答下列问题:
(1)A的结构简式为____________。
(2)B的化学名称为____________。
(3)C与D反应生成E的化学方程式为____________。
(4)由E生成F的反应类型为____________。
(5)G是分子式为____________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1mol的L可与2mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为___________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】块状大理石与过量的3mol·L-1盐酸反应制取二氧化碳气体,若要增大反应速率,采取的措施中不合理的是
A.加入氯化钠固体B.改用6molL-1盐酸C.改用粉末状大理石D.适当升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种典型的强氧化剂。
完成下列填空:
Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①![]() +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
②![]() +CuS+H+→Cu2++SO2↑+Mn2++H2O(未配平)
+CuS+H+→Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是______(填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
Ⅱ.在稀硫酸中,![]() 和H2O2也能发生氧化还原反应
和H2O2也能发生氧化还原反应
氧化反应:H2O22e![]() 2H++O2↑
2H++O2↑
还原反应:![]() +5e+8H+
+5e+8H+![]() Mn2++4H2O
Mn2++4H2O
(2)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为________。
(3)已知:2KMnO4+7H2O2+3H2SO4![]() K2SO4+2MnSO4+6O2↑+10H2O,则被1 mol KMnO4氧化的H2O2是______mol。
K2SO4+2MnSO4+6O2↑+10H2O,则被1 mol KMnO4氧化的H2O2是______mol。
Ⅲ.高锰酸钾溶液与硫化亚铁有如下反应:10FeS+6KMnO4+24H2SO4![]() 3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O
3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O
(4)若上述反应前后固体的质量减少了2.8 g,则硫元素与KMnO4之间发生电子转移的数目为____________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,不正确的是
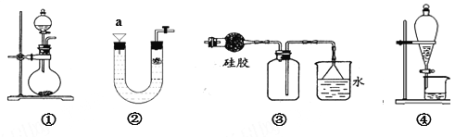
A.图①可用于实验室制备少量Cl2或NH3
B.可用从a处加水的方法检验装置②的气密性
C.实验室也可以用装置③收集HCl气体
D.装置④可用于苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 为原子序数依次增大的四种元素,
为原子序数依次增大的四种元素,![]() 和
和![]() 具有相同的电子构型;
具有相同的电子构型;![]() 、
、![]() 为同周期元素,
为同周期元素,![]() 核外电子总数是最外层电子数的3倍;
核外电子总数是最外层电子数的3倍;![]() 元素最外层有一个未成对电子。回答下列问题:
元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_______(填元素符号),其中![]() 原子的核外电子排布式为_________。
原子的核外电子排布式为_________。
(2)单质![]() 有两种同素异形体,其中沸点高的是______(填分子式),原因是_____________;
有两种同素异形体,其中沸点高的是______(填分子式),原因是_____________;![]() 和
和![]() 的氢化物所属的晶体类型分别为__________和__________。
的氢化物所属的晶体类型分别为__________和__________。
(3)![]() 和
和![]() 反应可生成组成比为1:3的化合物
反应可生成组成比为1:3的化合物![]() ,
,![]() 的立体构型为________,中心原子的杂化轨道类型为______________。
的立体构型为________,中心原子的杂化轨道类型为______________。
(4)化合物![]() 的立体构型为_________,中心原子的价层电子对数为_______,单质
的立体构型为_________,中心原子的价层电子对数为_______,单质![]() 与湿润的
与湿润的![]() 反应可制备
反应可制备![]() ,其化学方程式为______________。
,其化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017北京]SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
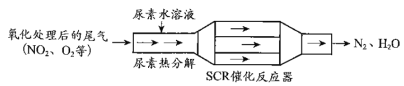
① 尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式:____________。
② 反应器中NH3还原NO2的化学方程式:____________。
③ 当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:________。
④ 尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 g·mol 1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是________。
(2)NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。
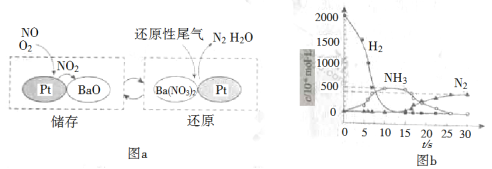
① 通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是_________。
② 用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是__________。
③ 还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:_______![]() □15NNO+□H2O
□15NNO+□H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两个电解池均以Pt为电极且互相串联。甲池盛有AgNO3溶液,乙池盛有一定量的某盐溶液,通电一段时间后,测得甲池阴极质量增加2.16g,乙池电极析出0.24g金属,则乙池中溶质可能是
A. CuSO4 B. MgSO4 C. Al(NO3)3 D. Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com