
| A. | 低碳生活就是节能减排,使用太阳能等代替化石燃料,可减少温室气体的排放 | |
| B. | 新能源的优点主要是资源丰富、可再生、没有或很少有污染 | |
| C. | 氢能的优点热值高、资源丰富、燃烧产物无污染;缺点是储存和运输困难 | |
| D. | 高纯度的硅单质广泛用于制作光导纤维 |
分析 A.“低碳生活”就是减少二氧化碳的排放,从而减缓温室效应;
B.新能源通常是环境友好型能源;
C.氢气是一种新能源,氢气燃烧产物为水无污染;
D.光导纤维的主要成分为二氧化硅.
解答 解:A.“低碳生活”就是通过各种手段、方法,尽量减少二氧化碳的排放,从而减缓温室效应,故A正确;
B.新能源相对于化石燃料来讲,资源丰富、可以再生、污染轻,对环境友好,故B正确;
C.氢气是一种新能源.氢气热值高,水作为其原料,资源实在太丰富了,氢气燃烧产物为水无污染,故C正确;
D.高纯度的硅单质广泛用于制作太阳能电池板,光导纤维是二氧化硅,故D错误.
故选D.
点评 本题考查了化石燃料使用的利弊,新能源的开发和利用,题目难度不大,通过本题可以培养学生节约能源,爱护环境,树立可持续发展的能源观念.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸氢钠稀溶液 | B. | 硝酸钠溶液 | C. | 醋酸钠溶液 | D. | 硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
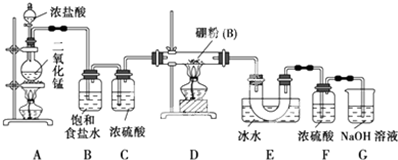
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
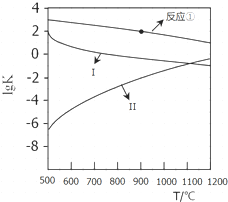 用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应.
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
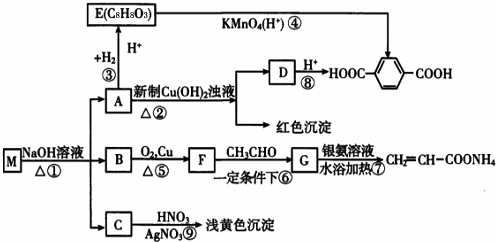
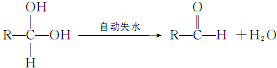
 ;E:
;E: ;G:CH2=CHCHO.
;G:CH2=CHCHO. .
. (写一种).
(写一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为SiO2 | B. | 熔化时共价键断裂 | ||
| C. | 属于酸性氧化物 | D. | 1mol SiO2中含有4 mol Si-O键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com