
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1。下列有关X的说法中不正确的是 ( )
A.X能形成化学式为X(OH)3的碱
B.X能与某些金属元素形成化合物
C.X原子的最外层电子数和核电荷数肯定为奇数
D.X可能形成化学式为KXO3的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学反应速率的认识正确的是
A.H+和OH—的反应活化能接近于零,反应几乎在瞬间完成
B.对于任何化学反应来说,反应速率越大,反应现象就越明显
C.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大
D.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,将一定量的冰醋酸(无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示。

请完成下列问题:
(1)上述a、b、c三点对应醋酸的电离程度最大的是 (填“a”、“b”、“c”),三点对应溶液中c(OH-)由大到小的顺序为 。
(2)c点对应的溶液中c(H+)与c(CH3COO-)+c(OH-)的关系为前者 (填“大于”“小于”“等于”)后者。
(3)从a点到b点,溶液中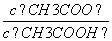 的比值 (填“增大”、“减小”、“等于”)。
的比值 (填“增大”、“减小”、“等于”)。
(4)25 ℃时,体积均为100 mL 、pH=m的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示。则稀释前两溶液中c(OH-)= , HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。

(5)若用pH试纸进行实验,你能否区分上述HX和CH3COOH两种酸溶液?若能,请简述操作过程;若不能,请说明理由。 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于碱金属的电子结构和性质的叙述中不正确的是( )
A.碱金属原子最外层都只有一个电子,在化学反应中容易失去
B.都是强还原剂
C.都能在O2中燃烧生成过氧化物
D.都能与水反应生成碱
查看答案和解析>>
科目:高中化学 来源: 题型:
上图为元素周期表截取的短周期的一部分,即 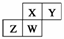 。 四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )
。 四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )
A.原子半径:W>Z>Y>X
B.气态氢化物 的稳定性:Z>W>X>Y
的稳定性:Z>W>X>Y
C.W的最高正化合价与负化合价的绝对值可能相等
D.Z的最高价氧化物的水化物可能为强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是( )
A.元素A、B组成的化合物可能是NH3
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应
C. C、D、E的半径:C>D>E
D.化合物AE与CE具有相同类型的化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
将一块银白色 的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是 ( )
的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是 ( )
A.表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠
B.“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液
C.最后变成碳酸钠粉末
D.该过程的所有化学反应均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废气中的氮氧化物(如NO、NO2等 ,用通式NOx表示)是主要的大气污染物之一.为了保护环境,
,用通式NOx表示)是主要的大气污染物之一.为了保护环境,
工业上常通入氨气与之发生如下反应:NOx+NH3—→N2+H2O来消除污染.有关此反应,下列说法中错误
的是 ( )
A.N2既是氧化产物又 是还原产物
是还原产物
B.当x=1时,每生成2.5 mol N2,被氧化的气体有3 mol
C.当x=2时,有1 mol气体被还原,转移电子4 mol
D.反应通式配平表示为:6NOx+4xNH3===(3+2x)N2+6xH2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com