
 .
. 分析 D的分子式为C8H7NO,其同分异构体满足①红外光谱检测表明分子中含有氰基(-CN);②1H-NMR谱检测表明分子中有苯环,且苯环上有两种不同化学环境的氢原子,即苯环上有两个处于对位的基团,据此写出符合条件的D的结构简式.
解答 解:D的分子式为C8H7NO,其同分异构体满足:①红外光谱检测表明分子中含有氰基(-CN);②1H-NMR谱检测表明分子中有苯环,且苯环上有两种不同化学环境的氢原子,即苯环上有两个处于对位的基团,则符合条件的D的结构简式为: ,
,
故答案为: .
.
点评 本题考查同分异构体的书写方法,题目难度不大,明确常见有机物组成、结构为解答关键,注意掌握同分异构体的书写原则,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:实验题
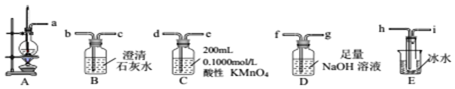
| 熔点/℃ | 沸点/℃ | 溶解性 | 颜色状态 | 密度g/cm3 | |
| 乙醇 | -114.1 | 78.3 | 与水、有机溶剂互溶 | 无色液体 | 0.79 |
| 乙醚 | -116.2 | 34.5 | 不溶于水,易溶于有机溶剂 | 无色液体 | 0.7135 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C7H8与C6H6互为同系物 | |
| B. | 由乙酸与乙醇制备乙酸乙酯的反位属于加成反位 | |
| C. | C3H6Br2有4种同分异构体 | |
| D. | 油脂在人体内最终分解为甘油和高级脂肪酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用K2FeO4代替Cl2处理饮用水,既有杀菌消毒作用,又有净水作用 | |
| B. | 古有“青蒿一握,以水二升渍,绞取汁”,今用乙醚从黄花蒿中提取青蒿素是利用氧化还原反应原理 | |
| C. | 面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物合物,也属于离子化合物,其阴阳离子冷数比为2:l,过氧化苯甲酞属于有机物 | |
| D. | 二氧化硫有毒,产禁将其添加到任何食品和饮料中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
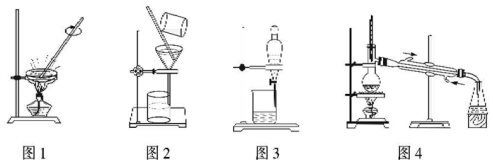
| A. | 用图1所示装置蒸发FeCl3溶液制得无水FeCl3 | |
| B. | 用图2所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 | |
| C. | 用图3所示装置从CH3OH与C2H5OH的混合物中分离出乙醇 | |
| D. | 用图4所示装置从CH3COOH与CH3COOC2H5的混合物中分离出乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
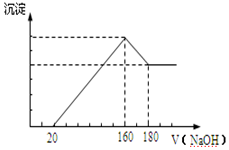 已知A、B、C、D、X、Y、Z七种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数比Y的最外层电子数多1.C原子的最外层电子数是次外层电子数的3倍,D原子半径在同周期中除稀有气体外最大,X是同周期中简单离子半径最小的元素.请回答下列问题:
已知A、B、C、D、X、Y、Z七种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数比Y的最外层电子数多1.C原子的最外层电子数是次外层电子数的3倍,D原子半径在同周期中除稀有气体外最大,X是同周期中简单离子半径最小的元素.请回答下列问题: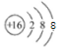 ,A与C形成的10电子分子的电子式为
,A与C形成的10电子分子的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单的离子半径:W>Z>Y>X | |
| B. | 五种元素中只有X存在同素异形体 | |
| C. | W和M形成的化合物是离子化合物 | |
| D. | 工业上采用电解W和Z形成的化合物制备W单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com