
 阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是( )
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是( )| A、1.0L 1.0mol?L-1H2SO4溶液中,H2SO4分子数为6.02×1023 |
| B、标准状况下,1mol SO3中所含的原子数为 6.02×1023 |
| C、32g S8单质中含有的S-S键个数为6.02×1023 |
| D、22.4L SO2中所含的分子数为6.02×1023 |
| 1 |
| 2 |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
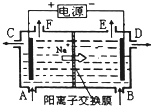 如图为阳离子交换膜法以石墨为电极电解饱和食盐水原理示意图.据图判断下列说法不正确的是( )
如图为阳离子交换膜法以石墨为电极电解饱和食盐水原理示意图.据图判断下列说法不正确的是( )| A、从E口逸出的气体是H2 |
| B、从F口逸出的气体是Cl2 |
| C、标准状况下,生成22.4LCl2的同时有2molNaOH生成 |
| D、从C口流出的是NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
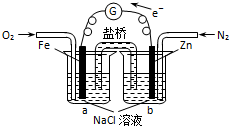 根据如图,下列判断中正确的是( )
根据如图,下列判断中正确的是( )| A、该装置将电能转化为化学能 |
| B、烧杯a中的溶液pH降低 |
| C、Fe电极发生了氧化反应 |
| D、烧杯b中发生的反应为Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、装置①中,c为阴极,d为阳极 |
| B、装置②可用于收集H2,CO2,O2,NO等气体 |
| C、装置③中的X为CCl4时,可用于吸收氯化氢气体,并防止倒吸 |
| D、装置④可用于收集氨气,并吸收尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,5.6 L一氧化氮和5.6L氧气混合后的分子总数为0.5NA |
| B、在H2O2+Cl2═2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 |
| C、1 mol乙烷分子中含有8NA个共价键 |
| D、58.5 g的氯化钠固体中含有NA个氯化钠分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将①中所得浊液过滤,所得滤液中含少量Mg2+ |
| B、浊液中存在溶解平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq) |
| C、实验②和③均能说明Fe(OH)3比Mg(OH)2难溶 |
| D、NH4Cl溶液中的NH4+可能是④中沉淀溶解的原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向溶液中加入少量KCl晶体 |
| B、向溶液中加入一定量KCl溶液 |
| C、向溶液中加少量AgNO3固体 |
| D、向溶液中滴加几滴1 mol?L-1FeCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com