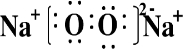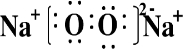���ϱ��е�ʵ����Ԫ�����ڱ����ֱ߽磬���ڱ�����ʵ�߲�ȫԪ�����ڱ��߽磬�����������ͷǽ����ķֽ��ߣ�����Ӱ������Ԫ�����ڵ��壮
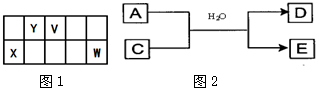
��A��B��C��D��E���Ƕ�����Ԫ�أ�ԭ��������������A��B����ͬһ���ڣ�C��D��Eͬ����һ���ڣ�C��B�ɰ�ԭ�Ӹ�����2��l��1��1�ֱ��γ��������ӻ�������ң�Aԭ�ӵ������������ȴ������Ӳ��3����E�ǵؿ��к�����ߵĽ���Ԫ�أ�����������Ϣ�ش��������⣺

��1��DԪ�������ڱ��е�λ����
��������IIA��
��������IIA��
������BԪ�ؼ����ӽṹʾ��ͼ
�������ʵĵ���ʽ��
��2��A��B��C��D��E����Ԫ�ص�ԭ�Ӱ뾶��С�����˳���ǣ���Ԫ�ط�����д��
O��N��Al��Mg��Na
O��N��Al��Mg��Na
��3��E�ĵ��ʼ��뵽C������������Ӧ��ˮ�������Һ�У�������Ӧ�����ӷ���ʽ��
2Al+2OH-+2H2O=2AlO2-+3H2��
2Al+2OH-+2H2O=2AlO2-+3H2��
��4�������Ƚ�D��E������ǿ����ʵ�鷽����
þ����ˮ���Է�Ӧ����������þ����������������ˮ����Ӧ
þ����ˮ���Է�Ӧ����������þ����������������ˮ����Ӧ
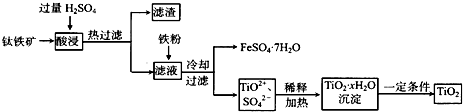
��5��E�ĵ��ʡ�ʯī�Ͷ������ѣ�TiO
2����������ϣ������·�Ӧ�õ������ֻ������������Ԫ����ɣ��Ҷ��������մɲ��ϣ��ڻ���͵���������ҪӦ�ã��䷴Ӧ����ʽΪ
��


 TiCl4+______����֪�÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1��1������һ������Ϊ______��
TiCl4+______����֪�÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1��1������һ������Ϊ______��