
| 锌的质量/g | 锌的形状 | 温度/℃ | 溶解于酸所花的时间/s |
A | 2 | 薄片 | 5 | 400 |
B | 2 | 薄片 | 15 | 200 |
C | 2 | 薄片 | 25 | 100 |
D | 2 | 薄片 | 35 | 40 |
E | 2 | 薄片 | 45 | 25 |
F | 2 | 粉末 | 15 | 5 |
试求:(1)画一幅以时间对温度的曲线图(纵轴表示时间,横轴表示温度)。
(2)利用所画的曲线图,关于温度影响反应速率你能得出什么结论?_____________________________________________________________________
(3)20 ℃时,2 g锌片溶解于酸中需花多少时间?______________________
(4)对比结果B与F,解释F为什么那么快?________________________________________
科目:高中化学 来源: 题型:
| 实验编号 | 锌的质量/g | 锌的形状 | 温度/℃ | 锌完全反应的时间/s |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 细小颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
| 锌的质量/g | 锌的形状 | 温度/℃ | 溶解于酸所花的时间/s | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
试求:
(1)画一幅以时间对温度的曲线图(纵轴表示时间,横轴表示温度).
(2)利用所画的曲线图,关于温度影响反应速率你能得出什么结论?
(3)20℃时,2g锌箔溶解于酸中需花多少时间?
(4)对比结果B与F,解释F为什么那么快?
查看答案和解析>>
科目:高中化学 来源: 题型:
(7分)在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
|
| 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于溶液的时间/s |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 细小颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
(1)t1= s
(2)总结并得出的关于温度影响反应速率的结论是
(3)t1 t4(填“>”或“<”),原因是
t2 t3(填“>”或“<”),原因是
(4)单位时间内消耗锌的质量mB、mE、mF从大到小的顺序为
查看答案和解析>>
科目:高中化学 来源:2010年山东省济南外国语学校高三上学期第二次质量检测化学卷 题型:填空题
(7分)在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
| | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于溶液的时间/s |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 细小颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖北省高三11月联考化学试卷 题型:实验题
(8分)在锌与盐酸反应的实验中,某学生得到的结果如下表所示:
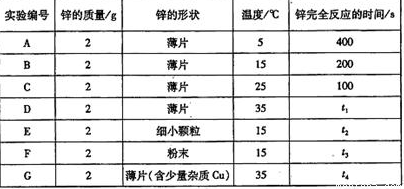
(1)t1= s。
(2)根据表中数据得出关于温度影响反应速率的结论是 。
(3)t1 t4(填“>”、“<”、“=”),原因是 。
(4)t2 t3(填“>”、“<”、“=”),原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com