
从下列实验事实所列出的相应结论不正确的是
实 验事实 | 结 论 | |
① | SO2使酸性高猛酸钾溶液褪色 | 可证明SO2有漂白性 |
② | 浓盐酸可除去烧瓶内残留的MnO2,稀硝酸可除去试管内壁的银镜,用硫磺粉处理洒落的金属汞 | 都发生了氧化还原反应 |
③ | 取少Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀,再滴加稀盐酸,沉淀不溶解 | 证明Na2SO3己氧化变质 |
④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的气体,另取该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
⑤ | 在某溶液中加入适量新制饱和氯水,再加入CCl4震荡,CCl4层呈橙红色 | 该溶液一定有Br-存在 |
A.①③④ B.②③⑤ C.④⑤ D.③④
科目:高中化学 来源:2017届山东省日照市高三上学期期中化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.6.0 g SiO2晶体中含有的分子数为0.1NA
B.3.2g S2和S4的混合物中所含硫原子数一定为0.2NA
C.标准状况下,22.4 L NO和11.2 L O2混合后气体的分子总数小于NA
D.在反应KClO3+6HCl=KCl+3C12↑+3H2O中,当得到标准状况下67.2 L Cl2时,反应中转移的电子数为6NA
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上模拟四化学卷(解析版) 题型:填空题
【化学-物质结构与性质】
配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题。
(1)写出元素D在周期表中的位置是 ,B原子的外围电子排布图 。E原子的核外有 种不同运动状态的电子,B和C的第一电离能大小关系 。(用元素符号表示)
(2)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,画出原子个数比为1:1的化合物的电子式 ,两种化合物可任意比互溶,解释其主要原因为 。
(3)该配位化合物的化学式为 。
(4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为 。
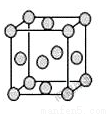
(5)已知E的晶胞结构如图所示,此晶胞立方体的边长为a cm,E单质的密度为pg.cm-3,则阿伏伽德罗常数为 (用a、p表示)。该晶胞配位数为 ,EDC4常作电镀液,其中DC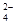 的空间构型是 ,其中D原子的杂化轨道类型是 。若电解EDC4的水溶液,则电解总反应的化学方程式为 。
的空间构型是 ,其中D原子的杂化轨道类型是 。若电解EDC4的水溶液,则电解总反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
在一定温度下,某浓度的酸与金属锌反应生成NO2和NO,两者的物质的量之比为1: 3, 则要使I mol金属锌完全反应,反应过程中消耗HNO3的物质的量为
A.2.4 mol B.2.6 mol C.2.8 mol D.3.2 mol
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
下列实验过程始终无明显现象的是
A. CO2气体通入Ba(NO3)2溶液中 B. NO2气体通入FeSO4溶液中
C. H2S气体通入CuSO4溶液中 D. HCl气体通入NaSiO3溶液中
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:实验题
金属及其化合物在生产中用途广泛。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶练铜的工艺流程如下:
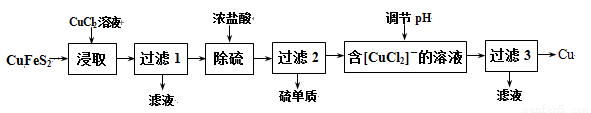
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有 ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为 。
Ⅱ.利用生产硼砂 的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
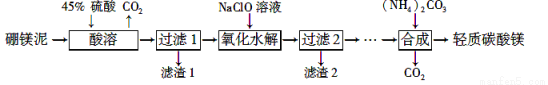
(1) 写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式 。
(2) 滤渣2的主要成分有MnO2和_____________,写出生成MnO2的离子方程式____________________。
(3)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是________________________(只需写出相应的化学方程式)。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
少量铁片与100mL 0.01mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加KN O3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaC
O3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaC l溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L盐酸
l溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L盐酸
A.①⑥⑦ B.③⑤⑧ C.③⑦⑧ D.③④⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的作用,下列有关说法不正确的是
A.硅酸钠的水溶液俗称水玻璃,可用作木材防火剂
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
C.含磷污水是很好的肥料,可灌溉庄稼,可直接排放到自然界水体中
D.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二11月月考化学试卷(解析版) 题型:选择题
接触法制硫酸中,进入接触室的气体必须净化、干燥,其主要原因是( )
A.防止催化剂中毒 B.提高反应效率
C.提高SO2转化率 D.防止环境污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com