
| 6.72L |
| 22.4L/mol |
| n |
| V |
| 6.72L |
| 22.4L/mol |
| n |
| V |
| 0.3mol |
| 0.5L |
| 88×1.4g |
| 56 |
| 2.2g |
| 44g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 3n |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
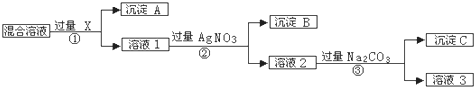
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解NaNO3溶液,在阴极上和阳极上析出产物的物质的量之比为2:1 |
| B、电解CuSO4溶液一段时间后,再加入一定质量Cu(OH)2,溶液能与原溶液完全一样 |
| C、电解硫酸钠溶液时,Na+向阳极移动 |
| D、电解KOH溶液,实质上是电解水,故溶液pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水的电离度α(25℃)>α(35℃) |
| B、c(H+)随着温度的降低而升高 |
| C、在35℃时,纯水中c(H+)>c(OH-) |
| D、水的电离过程是吸热过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
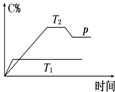 在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铝是电解质,可电解其水溶液获得金属铝 |
| B、二氧化硅具有导电性,可用于生产光导纤维 |
| C、SO2具有漂白性,可用于将银耳漂白为“雪耳” |
| D、小苏打可与酸反应,可用作治疗胃酸过多的药剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com