
科目:高中化学 来源: 题型:
用系统命名法命名下列烷烃
(1) 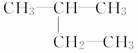 ______________________________________________;
______________________________________________;
(2) 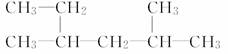 ___________________________________;
___________________________________;
(3) 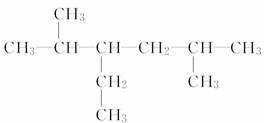 _______________________________;
_______________________________;
(4) 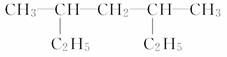 ___________________________________;
___________________________________;
(5) 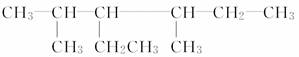 __________________________。
__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液,其中可能存在的离子有:Na+、Ag+、Ba2+、Fe3+、Al3+、AlO2-、
S2-、SO32-、CO32-、SO42-,现取该溶液进行实验,实验结果如下:
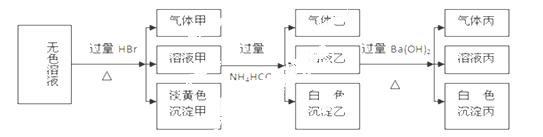
试回答下列问题:
(1)生成沉淀甲的离子方程式为: 。
(2)由溶液甲生成沉淀乙的离子方程式为 。
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表(表中每一行对应正确即可得分)
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | 检验CO2 | 澄清石灰水 | 溶液变浑浊 |
(4)综上所述,该溶液肯定存在的离子有: 。
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,将1molM和1molN气体充入2L恒容密闭容器,发生反应M(g)+ N(g) xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。下列说法正确的是( )
xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。下列说法正确的是( )
A.反应方程式中的x=1
B.t2时刻改变的条件是使用催化剂
C.t3时刻改变的条件是移去少量物质Q
D.t1~t3间该反应的平衡常数均为4
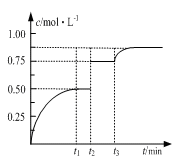
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2A2(g)+B2(g) 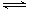 2C
2C 3(g);△H=-Q1 kJ/mol(Q1>0), 在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为w mol·L-1,放出热量为Q2 kJ。
3(g);△H=-Q1 kJ/mol(Q1>0), 在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为w mol·L-1,放出热量为Q2 kJ。
(1)达到平衡时, A2的转化率为________。
A2的转化率为________。
(2)达到平衡后,若向原容器中通入少量的氩气,A2的转化率将________(填“增大“、“减小”或“不变”)
(3)若在原来的容器中,只加入2mol C3,500℃时充分反应达平衡后,吸收热量Q3 kJ,C3浓度 (填>、=、<)w mol·L-1,Q1、Q2、Q3 之间满足何种关系
之间满足何种关系
(4)能说明该反应已经达到平衡状态的是 。
a.v(C3)=2 v (B2); b.容器内压强保持不变 
 c.2v逆(A2)=v正(B2) d.容器内的密度保持不变
c.2v逆(A2)=v正(B2) d.容器内的密度保持不变
(5)改变某一条件,得到如图的变化规律 (图中T表示温度,n表示物质的量),可得出的结论正确的是 ;
(图中T表示温度,n表示物质的量),可得出的结论正确的是 ;
a.反应速率c>b>a
b.达到平衡时A2的转化率大小为:b>a>c
c.T2>T1
d. b点A2和B2的物质的量之比为2:1
(6)若将上述容器改为恒压容器(反应前体积相同),起 始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 (填“>”、“<”或“=”)。
始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 (填“>”、“<”或“=”)。
(7)下列措施可以同时提高反应速率和B2的转化率是(填选项序号) 。
a.选择适当的催化剂 b .增大压强 c.及时分离生成的C3 d.升高温度
.增大压强 c.及时分离生成的C3 d.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氯气或氯水的叙述不正确的是
A.氯气能使润湿的淀粉碘化钾试纸变蓝
B.新制的氯水呈黄绿色是因为在溶液中溶有氯气分子
C.与久置氯水不同,在新制氯水中加入硝酸银溶液后无白色沉淀
D.氯水久置后,会使溶液酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应的实质和相应的规律是
A.化合价的升降,化合价的升高和降低的总数相等
B.电子的转移,得电子总数和失电子总数相等
C.得氧和失氧,氧原子数目不变
D.物质的种类发生改变,质量守恒定律
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数约为6.02×1023mol—1,下列叙述中正确的是( )
A.常温常压下,18.0 g重水(D2O)所含的电子数约为10×6.02×1023
B.室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023
C.标准状况下,22.4 L苯所含的分子数约为6.02×1023
D.标准状况下,a L乙烷气体中的所含共价键数约为(a/22.4)×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
在100℃时,将0.40 mol NO2气体充入2 L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)(mol) | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)(mol) | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
下列说法中正确的是( )
A.反应开始20 s内NO2的平均反应速率是0.0025 mol·L-1·s-1
B.80 s时混合气体的颜色与60 s时颜色相同,比40 s时的颜色深
C.80 s时向容器内加0.32 mol He,同时将容器扩大为4 L,则平衡不移动
D.若起始投料为0.20 mol N2O4,相同条件下达到平衡,则各组分的含量与原平衡相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com