
 2NH3��g��������ӦΪ���ȷ�Ӧ���ﵽƽ���ֻ�ı�һ������ʱ��������ƽ��Ĺ��̡���д���и��գ�����дͼ��ţ���
2NH3��g��������ӦΪ���ȷ�Ӧ���ﵽƽ���ֻ�ı�һ������ʱ��������ƽ��Ĺ��̡���д���и��գ�����дͼ��ţ���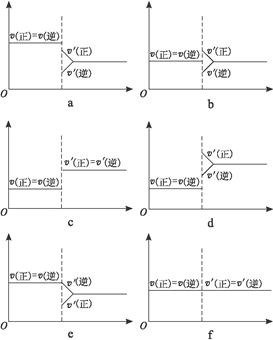



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g������X2��Y2��Z����ʼ�ܶȷֱ�Ϊ0.10 mol/L��0.30 mol/L��0.20 mol/L����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����( ��
2Z(g������X2��Y2��Z����ʼ�ܶȷֱ�Ϊ0.10 mol/L��0.30 mol/L��0.20 mol/L����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����( ��| A��c(Z��="0.50" mol/L | B��c(Y2��="0.50" mol/L |
| C��c(X2��="0.20" mol/L | D��c(Y2��="0.60" mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
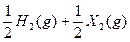

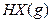 ��ƽ�ⳣ��Ϊ9������1.0 mol��HX(g)ͨ�����Ϊ1.0 L���ܱ������У��ڸ��¶�ʱHX(g)�����ֽ��ʽӽ���
��ƽ�ⳣ��Ϊ9������1.0 mol��HX(g)ͨ�����Ϊ1.0 L���ܱ������У��ڸ��¶�ʱHX(g)�����ֽ��ʽӽ���| A��10% | B��18% | C��20% | D��40% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g)����֪X2��Y2��Z����ʼ���ֱ�Ϊ0.10 mol��0.3 mol�� 0.2 mol��һ�������´ﵽƽ��ʱ������ֵ����ʵ����п����ǣ� ��
2Z(g)����֪X2��Y2��Z����ʼ���ֱ�Ϊ0.10 mol��0.3 mol�� 0.2 mol��һ�������´ﵽƽ��ʱ������ֵ����ʵ����п����ǣ� ��| A��ZΪ0.3 mol | B��Y2Ϊ0.35 mol | C��X2Ϊ0.2 mol | D��ZΪ0.4 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)+D(g)
C(g)+D(g)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A������1.369 g��L-1 | B������2.054 g��L-1 |
| C����1.369 g��L-1��2.054 g��L-1֮�� | D������2.054 g��L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
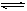 2�Σ������ﵽƽ�⣬��ʱ��������ڻ��������ܶȱ�ԭ������1��3���¶Ⱥ�ѹǿ���䣩�����㣺
2�Σ������ﵽƽ�⣬��ʱ��������ڻ��������ܶȱ�ԭ������1��3���¶Ⱥ�ѹǿ���䣩�����㣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3��ƽ����ϵ�У�����O2��Ũ�ȣ�����ƽ�������˵������ȷ���ǣ� ��
2SO3��ƽ����ϵ�У�����O2��Ũ�ȣ�����ƽ�������˵������ȷ���ǣ� ��| A������Ӧ�������� | B���淴Ӧ���ʼ�С |
| C��SO2��ת�������� | D��SO3��Ũ��һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 N2��3H2����ƽ��ʱ��N2�����ʵ�������Ϊa %��ά��������������¶����䣬�ֱ�ͨ�����м������ʣ��ﵽƽ��ʱ��������N2�����ʵ���������Ϊa %���ǣ���������
N2��3H2����ƽ��ʱ��N2�����ʵ�������Ϊa %��ά��������������¶����䣬�ֱ�ͨ�����м������ʣ��ﵽƽ��ʱ��������N2�����ʵ���������Ϊa %���ǣ���������| A��3mol H2��1mol N2 | B��4mol NH3 |
| C��2mol N2��6mol H2 | D��2mol NH3��1mol N2��3mol H2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com