
分析 n(NaCl)=$\frac{23.4g}{58.5g/mol}$=0.4mol,n(H2SO4)=0.3mol
(1)微热时发生发生NaCl+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HCl↑,据此进行计算;
(2)充分强热发生2NaCl+H2SO4(浓)$\frac{\underline{\;加热\;}}{\;}$Na2SO4+2HCl↑,据此进行计算.
解答 解:n(NaCl)=$\frac{23.4g}{58.5g/mol}$=0.4mol,n(H2SO4)=0.3mol
(1)NaCl+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HCl↑,注意计算时已不足的作为计算对象,
1 1
0.3 0.3
则:n(HCl)=0.3mol
答:可以生成HCl 0.3mol;
(2)2NaCl+H2SO4(浓)$\frac{\underline{\;加热\;}}{\;}$Na2SO4+2HCl↑,注意计算时已不足的作为计算对象,
2 2
0.4 0.4
则:n(HCl)=0.4mol
答:可以生成HCl 0.4mol.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应、物质的量关系、物质的量的相关计算公式为解答的关键,侧重分析与计算能力的考查,注意过量判断,题目难度不大.


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:推断题
 A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb;C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.
A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb;C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.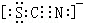 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
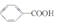 )和石灰的混合物得到一种液体,命名为苯.写出苯甲酸钠(
)和石灰的混合物得到一种液体,命名为苯.写出苯甲酸钠(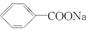 )与NaOH、生石灰共热生成苯的化学方程式:
)与NaOH、生石灰共热生成苯的化学方程式: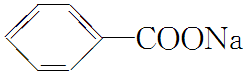 +NaOH
+NaOH  +Na2CO3.
+Na2CO3.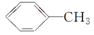 来制取
来制取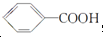 需要的试剂是KMnO4酸性溶液,下列物质属于苯的同系物且能被该试剂氧化的是d.
需要的试剂是KMnO4酸性溶液,下列物质属于苯的同系物且能被该试剂氧化的是d.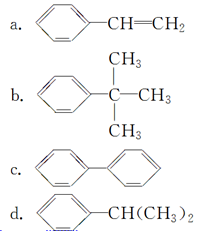
 .
.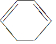 )脱去2mol氢原子变成苯却要放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).
)脱去2mol氢原子变成苯却要放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).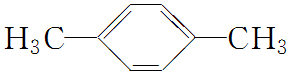 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4NO3 | B. | NaOH | C. | MgSO4 | D. | Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
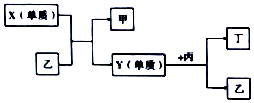 现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )| A. | 原子半径的大小:W<Y<Z<X | B. | 单质与H2化合的难易程度:X>Y | ||
| C. | 甲与丙反应不可能生成离子化合物 | D. | Z的最高价氧化物的水化物为强酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com