

 .
. .
. .
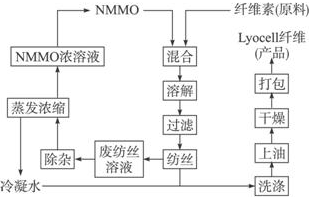
. 分析 (1)①从生产“Lyocell纤维”的工艺流程可看出NMMO可循环使用;
②从黏胶纤维的生产工艺可知,CS2中S元素、HCl中Cl元素成为不可再利用的物质;
③对环境污染越小越好;
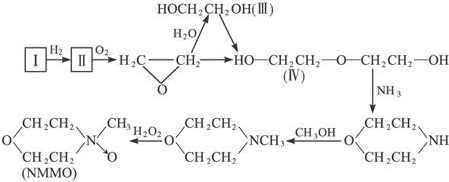
(2)化合物I可三聚为最简单的芳香烃,则I为CH2≡CH2,I和氢气发生加成反应生成II,化合物Ⅱ可使溴水褪色,则II为CH2=CH2,II被氧化生成环氧乙烷,环氧乙烷水解生成HOCH2CH2OH,HOCH2CH2OH发生取代反应生成HOCH2CH2OCH2CH2OH,HOCH2CH2OCH2CH2OH和NH3发生取代反应生成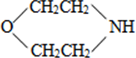 ,
,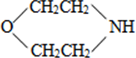 和甲醇发生取代反应生成
和甲醇发生取代反应生成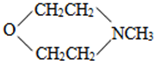 ,
, 和双氧水发生反应生成
和双氧水发生反应生成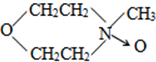 ,
,
①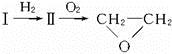 可推知:Ⅱ为CH2=CH2,则Ⅰ为CH≡CH,化合物Ⅰ也可聚合为在一定条件下具有导电性的高分子化合物,该高分子化合物为聚乙炔;
可推知:Ⅱ为CH2=CH2,则Ⅰ为CH≡CH,化合物Ⅰ也可聚合为在一定条件下具有导电性的高分子化合物,该高分子化合物为聚乙炔;
②化合物Ⅱ与氧气反应的原子利用率达100%,则二者反应生成环氧乙烷;
③Ⅲ(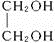 )和HOCH2CH2OCH2CH2OH均含2个OH,均具有醇的性质,可发生酯化反应,可与钠反应,可被氧化,可由卤代烃水解生成,可溶于水;
)和HOCH2CH2OCH2CH2OH均含2个OH,均具有醇的性质,可发生酯化反应,可与钠反应,可被氧化,可由卤代烃水解生成,可溶于水;
④ 和双氧水发生反应生成
和双氧水发生反应生成 .
.
解答 解:(1)①从生产“Lyocell纤维”的工艺流程可看出NMMO可循环使用,故答案为:NMMO;
②从黏胶纤维的生产工艺可知,CS2中S元素、HCl中Cl元素成为不可再利用的物质,故答案为:S、Cl;
③“Lyocell纤维”被誉为“21世纪的绿色纤维”,原因是该反应中产生废弃物少,环境污染小,故答案为:环境污染小;
(2)化合物I可三聚为最简单的芳香烃,则I为CH2≡CH2,I和氢气发生加成反应生成II,化合物Ⅱ可使溴水褪色,则II为CH2=CH2,II被氧化生成环氧乙烷,环氧乙烷水解生成HOCH2CH2OH,HOCH2CH2OH发生取代反应生成HOCH2CH2OCH2CH2OH,HOCH2CH2OCH2CH2OH和NH3发生取代反应生成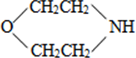 ,
,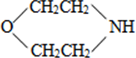 和甲醇发生取代反应生成
和甲醇发生取代反应生成 ,
, 和双氧水发生反应生成
和双氧水发生反应生成 ,
,
① 可推知:Ⅱ为CH2=CH2,则Ⅰ为CH≡CH,化合物Ⅰ也可聚合为在一定条件下具有导电性的高分子化合物,该高分子化合物为聚乙炔,其结构简式为:
可推知:Ⅱ为CH2=CH2,则Ⅰ为CH≡CH,化合物Ⅰ也可聚合为在一定条件下具有导电性的高分子化合物,该高分子化合物为聚乙炔,其结构简式为: ,
,
故答案为: ;
;
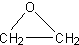
②化合物Ⅱ与氧气反应的原子利用率达100%,则二者反应生成环氧乙烷,反应方程式为2CH2═CH2+O2$→_{△}^{催化剂}$2 ,
,
故答案为:2CH2═CH2+O2$→_{△}^{催化剂}$2 ;
;
③A.Ⅲ、Ⅳ中都含有醇羟基,所以二者都可以发生酯化反应,故正确;
B.Ⅲ、IV都是有机物且都含有醇羟基,都可以被氧化,故错误;
C.Ⅲ、IV都是有机物且都含有醇羟基,都溶于水,故正确;
D.Ⅲ、Ⅳ中都含有醇羟基,所以都可以和Na反应生成氢气,故错误;
E.Ⅲ中含有两个羟基,所以和乙醇不是同系物,故错误;
F.Ⅲ可由卤代烃和NaOH的水溶液、加热而发生取代反应制备,故正确;
故选A、C、F;
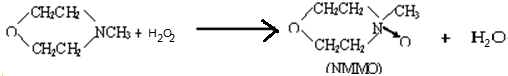
④ 和双氧水发生反应生成
和双氧水发生反应生成 ,反应方程式为
,反应方程式为 ,
,
故答案为: ;
;
点评 本题考查有机合成,为高频考点,根据反应前后物质结构变化确定反应类型,侧重考查学生分析推断能力,难点是生成NMMO的反应中断键和成键方式,题目难度不大.


科目:高中化学 来源: 题型:选择题
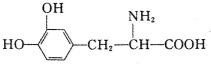
| A. | 常温下,不溶于水 | B. | 既可与酸反应,又可与碱反应 | ||
| C. | 遇FeCl3溶液无变化 | D. | 与溴水混合,溴水褪色,溶液分两层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1句 | B. | 2句 | C. | 3句 | D. | 4句 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
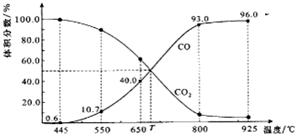 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、K+、Fe2+、NO3- | B. | OH-、Cl-、Na+、NH4+ | ||
| C. | Mg2+、K+、Cl-、NO3- | D. | Cu2+、NO3-、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铜溶液与铁粉反应:Cu2++Fe═Fe2++Cu | |
| B. | 稀 HNO3与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀H2SO4反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 碳酸钙与醋酸反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com