
【题目】由N、B等元素组成的新型材料有着广泛用途.
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造.由第二周期元素组成的与BCl3互为等电子体的阴离子为(填离子符号,填一个).
(2)氨硼烷(H3N→BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料.
①H3N→BH3中N原子的轨道杂化类型为 .
②Ti(BH4)3由TiCl3和LiBH4反应制得.基态Ti3+的未成对电子数有个,BH4﹣的立体构型是 . 写出该制备反应的化学方程式 .
③氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:3CH4+2 (HB=NH)3+6H2O→3CO2+6H3BNH3
与上述化学方程式有关的叙述不正确的是 . (填标号)
A.氨硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
(3)磷化硼(BP)是受到高度关注的耐磨材料.如图1为磷化硼晶胞. 
①磷化硼晶体属于晶体(填晶体类型),(填是或否)含有配位键.
②晶体中B原子的配位数为 .
(4)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是 .
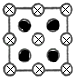
(5)图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置. 
【答案】
(1)CO32﹣或NO3﹣
(2)sp3;1;正四面体;TiCl3+3LiBH4=Ti(BH4)3+3LiCl;C
(3)原子;是;4
(4)B﹣N键键长大于C﹣C键键长,键能小,所以熔点低
(5)
【解析】解:(1)根据等电子体原理,原子数相同,价电子数也相同的粒子互为等电子体,所以由第2周期元素组成的与BCl3互为等电子体的阴离子为CO32﹣或NO3﹣ ,
所以答案是:CO32﹣或NO3﹣;
(2.)①H3N→BH3中N原子的价层电子对数为 ![]() =4,所以N原子的轨道杂化类型为sp3 , 所以答案是:sp3
=4,所以N原子的轨道杂化类型为sp3 , 所以答案是:sp3
②基态Ti3+的核外电子排布式为1s22s22p63s23p63d1 , 其未成对电子数是1. BH4﹣中B原子的价层电子对数为 ![]() =4,所以杂化方式为sp3杂化,则BH4﹣的立体构型为正四面体,Ti(BH4)3由TiCl3和LiBH4反应制得,反应的化学方程式为TiCl3+3LiBH4═Ti(BH4)3+3LiCl,所以答案是:1;正四面体;TiCl3+3LiBH4=Ti(BH4)3+3LiCl;
=4,所以杂化方式为sp3杂化,则BH4﹣的立体构型为正四面体,Ti(BH4)3由TiCl3和LiBH4反应制得,反应的化学方程式为TiCl3+3LiBH4═Ti(BH4)3+3LiCl,所以答案是:1;正四面体;TiCl3+3LiBH4=Ti(BH4)3+3LiCl;
③A.B一般是形成3个键,(H3BNH3)由六元环状化合物(HB=NH)3通过3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得,其中1个键是配位键,故A正确;
B.同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,这几种元素都是第二周期元素,它们的族序数分别是:第IIIA族、第IVA族、第VA族、第VIA族,所以它们的第一电离能大小顺序是I1(N)>I1(O)>I1(C)>I1(B),故B正确;
C.由CH4变为CO2 , 碳原子杂化类型由sp3转化为sp,反应前后碳原子的轨道杂化类型已经改变,故C错误;
D.CH4分子中价层电子对=σ 键电子对+中心原子上的孤电子对=4+ ![]() ×(4﹣4×1)=4,且不含孤电子对,所以其空间构型是正四面体,H2O中价层电子对个数=2+
×(4﹣4×1)=4,且不含孤电子对,所以其空间构型是正四面体,H2O中价层电子对个数=2+ ![]() ×(6﹣2×1)=4,且含有2个孤电子对,所以H2O的VSEPR模型为四面体,分子空间构型为V型,、CO2分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+
×(6﹣2×1)=4,且含有2个孤电子对,所以H2O的VSEPR模型为四面体,分子空间构型为V型,、CO2分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+ ![]() ×(4﹣2×2)=2,所以二氧化碳是直线型结构,故D正确,
×(4﹣2×2)=2,所以二氧化碳是直线型结构,故D正确,
所以答案是:C;
(3.)①在磷化硼晶体中,磷和硼原子之间通过共价键相互作用,结合性质可知其晶体类型为原子晶体,硼最外层有3个电子,但根据晶胞结构可知,每个硼和磷周围都有4个共价键,所以磷原子含有孤电子对,硼原子含有空轨道,它们之间存在配位键,所以答案是:原子;是;
②根据晶的结构图可知,每个磷原子周围有4个硼原子,所以配位数为4,所以答案是:4;
(4.)立方氮化硼结构和硬度都与金刚石相似,均为原子晶体,B﹣N键键长大于C﹣C键,键能小于C﹣C键,导致立方氮化硼熔点比金刚石低;所以答案是:B﹣N键键长大于C﹣C键键长,键能小,所以熔点低
(5.)晶体中B、N原子配位数均为4,涂“●”和画“×”分别标明B与N的相对位置为:  ,所以答案是:
,所以答案是:  .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列过程中发生氧化还原反应的是
A. Cu和稀HNO3反应 B. Fe的导电
C. NaHCO3受热分解 D. 实验室用NH4Cl和Ca(OH)2反应制取NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多卤代甲烷常作为有机溶剂,其中分子结构为正四面体的是 . 工业上分离这些多氯代甲烷的方法是 .
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式(不考虑立体异构).
(3)聚氯乙烯是生活中常用的塑料.工业生产聚氯乙烯的一种工艺路线如下: ![]()
反应①的化学方程式为 , 反应类型为;反应②的反应类型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面有关丙烷、丙烯、丙炔说法中正确的有( )
A.丙烷、丙烯、丙炔的结构式分别为 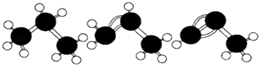
B.相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3:2:1
C.丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相对条件下密度逐渐增大
D.丙烷的碳原子空间结构是锯齿型的,不是简单的线性排列
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鸦片最早用于药物(有止痛、止泻、止咳的作用),长期服用会成瘾,使人体质衰弱,精神颓废,寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如下:  已知该物质的燃烧产物为CO2、H2O和N2 , 1mol该化和物完全燃烧消耗的O2的物质的量及在一定条件下与Br2发生苯环取代反应生成的一溴代物的同分异构体的种数分别为( )
已知该物质的燃烧产物为CO2、H2O和N2 , 1mol该化和物完全燃烧消耗的O2的物质的量及在一定条件下与Br2发生苯环取代反应生成的一溴代物的同分异构体的种数分别为( )
A.23.25mol 5
B.24.5mol 7
C.24.5mol 8
D.23.25mol 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示仪器可用于实验室制备少量无水FeCl3 , 仪器连接顺序正确的是( ) 
A.a﹣b﹣c﹣d﹣e﹣e﹣f﹣g﹣h
B.a﹣e﹣d﹣c﹣b﹣h﹣i﹣g
C.a﹣d﹣e﹣c﹣b﹣h﹣i﹣g
D.a﹣c﹣b﹣d﹣e﹣h﹣i﹣f
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
选项 | X | Y |
A | MgSO4 | CuSO4 |
B | AgNO3 | Pb(NO3)2 |
C | FeSO4 | Al2 (SO4)3 |
D | CuSO4 | AgNO3 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某些化学知识用图象表示,可以收到直观、简明的效果.下列图象所表示的化学知识中,明显不正确的是( )
A. 分散系的分类
分散系的分类
B. 稀释浓氢氧化钠溶液的过程
稀释浓氢氧化钠溶液的过程
C. 向碳酸钠溶液中逐滴滴加盐酸
向碳酸钠溶液中逐滴滴加盐酸
D. 向偏铝酸钠溶液中逐滴滴加盐酸
向偏铝酸钠溶液中逐滴滴加盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com