
【题目】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图1所示的关系,完成下列空白:

(1)向酚酞试液中加入化合物A的粉末,现象为_____________。
(2)单质甲与化合物B反应的离子方程式为_______________。
(3)向20mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。

①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_________。
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为________。
③由A、B可知,两次实验通入的CO2的体积比为__________。
【答案】
(1)溶液先变红后褪色,并有气泡生成;
(2)2Na+2H2O═2Na+ +2OH- +H2 ↑;
(3)①OH- +H+ =H2O、H+ +CO32- =HCO3-;②Na2CO3、NaHCO3;③3:10。
【解析】
试题分析:A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,甲与B反应是置换反应,甲与乙是化合反应,丙与乙也是化合反应,单质甲、含有甲元素的化合物A均与化合物B反应得到不同的单质,且两种单质反应又得到化合物B,应是Na、过氧化钠与水的反应,可推知甲是Na单质,乙为氧气,B是H2O,丙为氢气,C是NaOH,A是Na2O2。
(1)向酚酞试液中加入化合物Na2O2的粉末,过氧化钠与水反应生成氢氧化钠与氧气,氢氧化钠是溶液薄荷味红色,但过氧化钠具有漂白性,则现象为:溶液先变红后褪色,并有气泡生成,故答案为:溶液先变红后褪色,并有气泡生成;
(2)单质甲与化合物B反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑;
(3)曲线A、B,开始没有气体,加入一定体积盐酸后生成气体,生成气体的反应为:HCO3-+H+=H2O+CO2↑,若A中只有Na2CO3,开始发生CO32-+H+=HCO3-,前后两过程消耗HCl的体积相等,实际开始阶段消耗盐酸体积大于产生二氧化碳消耗的盐酸体积,故A曲线表明M中的溶质为NaOH、Na2CO3,B曲线中,前后消耗盐酸的体积之比为1:2,则曲线B表明M中溶质为Na2CO3、NaHCO3,且二者物质的量之比为1:1,
①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为:OH-+H+=H2O、H++CO32-=HCO3-,故答案为:OH-+H+=H2O、H++CO32-=HCO3-;
②由A图表明,加入60mL盐酸时开始产生二氧化碳,到75mL时二氧化碳的体积达最大,所以加入盐酸体积60mL~75mL时,是盐酸与碳酸氢钠反应,根据反应的关系式可知2n(Na2CO3)=n(HCl),而反应中n(HCl)>>2n(Na2CO3),所以原溶液的溶质为Na2CO3、NaOH,故答案为:Na2CO3、NaOH;
③曲线A生成二氧化碳消耗盐酸体积为(75-60)mL=15mL,曲线B生成二氧化碳消耗盐酸体积为(75-25)mL=50mL,由HCO3-+H+=H2O+CO2↑可知,则两次实验通入的CO2的体积之比=15mL:50mL=3:10,故答案为:3:10。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
【题目】已知可逆反应:M(g)+N(g)![]() P(g)+Q(g) △H> 0请回答下列问题
P(g)+Q(g) △H> 0请回答下列问题
(1)在某温度下,反应物的起始浓度分别为c(M)=1mol/L,c(N)=2.4mol/L;达到平衡后,M的转化率为60%,此时N的转化率为____________
(2)若反应温度升高,M的转化率 (填“增大”、“减小”或“不变”)
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4mol/L,c(N)=amol/L;达到平衡后,c(P)=2mol/L,a=____________
(4)若反应温度不变,反应物的起始浓度为c(M)=c(N)=bmol/L,达到平衡后,M的转化率为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
A.c1:c2=1:3B.X、Y的转化率不相等
C.平衡时,Y和Z的生成速率之比为3:2D.c1的取值范围为0<c1<0.14mo/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法与盐类水解无关的是
A. 粗盐在空气中易潮解 B. NH4Cl与ZnCl2用于金属焊接中除锈
C. 用热纯碱溶液去油污 D. 蒸干并灼烧FeCl3溶液得到Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是用自来水制备蒸馏水的实验装置图。
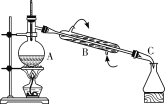
实验室蒸馏装置
(1)填写仪器名称:A:______________; B:________________; C:________________。
(2)图中有一处错误,请指出:________________________。
(3)蒸馏时,瓶中要先加几块沸石,其目的是________________。
(4)蒸馏时,取________℃的产品即可获得蒸馏水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol L气体和3 mol M气体混合,发生如下反应:2L(g)+3M(g)![]() xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
(1)10 s末L的物质的量浓度为_____________。
(2)前10 s内用M表示的化学反应速率为_____________。
(3)化学方程式中x值为_____________。
(4)在恒温恒容条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
(5)在恒温恒压条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,Q与水反应的化学方程式为_____________。
(2)NaCN超标的电镀废水可用两段氧化法处理:
1.NaCN与NaClO反应,生成NaOCN和NaCl
2.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
①写出第二次氧化时发生反应的离子方程式。
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成____________和H2O。
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO_________g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.钢铁在潮湿的空气中容易生锈
C.实验室中常用排饱和食盐水的方法收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合,离子方程式正确的是
A. CO32— + Ba2+ → BaCO3↓
B. HCO3— + OH— → H2O + CO32—
C. HCO3— + Ba2+ + OH— → H2O + BaCO3↓
D. 2HCO3— + Ba2+ + 2OH— → BaCO3↓+ 2H2O + CO32—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com