
| A�� | A��BԪ���γɵ�һϵ�л������У�����AԪ���������������ֵΪ25% | |
| B�� | ����Ԫ���е縺��������B | |
| C�� | C���γɵ���̬�⻯�����ͬ����Ԫ�ص���̬�⻯���зе���� | |
| D�� | ����Ԫ���е�һ��������С����D |
���� ԭ�������������������Ԫ��A��B��C��D�ֱ��ڵ�һ���������ڣ�����Aԭ�Ӻ���һ�����ӣ���AΪ��Ԫ�أ�Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬����������6�����ӣ���BΪ̼Ԫ�أ�B��C���γ����������ͷ��ӣ���CΪ��Ԫ�أ�Dԭ����Χ�����Ų�Ϊ3d104s1����DΪͭԪ�أ��ݴ˽��н��
��� �⣺ԭ�������������������Ԫ��A��B��C��D�ֱ��ڵ�һ���������ڣ�����Aԭ�Ӻ���һ�����ӣ���AΪ��Ԫ�أ�Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬����������6�����ӣ���BΪ̼Ԫ�أ�B��C���γ����������ͷ��ӣ���BΪClԪ�أ�Dԭ����Χ�����Ų�Ϊ3d104s1����DΪͭԪ�أ�
A��C��H�γɵĻ�����Ϊ�������к���������Ϊ���飬�������Ϊ��$\frac{4}{16}$��100%=25%����A��ȷ��
B������Ԫ������Ԫ�طǽ�������ǿ����縺�����B����
C��CΪClԪ�أ�λ�ڢ���A�壬����Ԫ���У�HF�е���ߣ�������̬�⻯�����Է�������Խ���Ӽ�������Խ����е�Խ�ߣ�����HCl�ķе���ͣ���C��ȷ��
D��ͭΪ����������Ϊ�ǽ���������ͭ�ĵ�һ��������С����D��ȷ��
��ѡB��
���� ���⿼����ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ����Ŀ�Ѷ��еȣ��ƶ�Ԫ��Ϊ���ؼ���ע������ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ������������ѧ���ķ���������������������


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������Ũ�������ƿ������� | |
| B�� | ���õ��ȡ���ϫ����Դ�����ʯȼ�� | |
| C�� | ʹ�ÿɽ������ϼ��١���ɫ��Ⱦ�� | |
| D�� | ѡ�ò���������ϴ�Ӽ���ֹ������Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | Cl2O | ClO2 | Cl2O7 |
| �е�/�� | 3.8 | 11.0 | 82.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl�����к���Na+��Cl-������NaCl�����ܵ��� | |
| B�� | CO2����ˮ�ܵ��磬����CO2�ǵ���� | |
| C�� | BaSO4������ˮ��BaSO4�Ƿǵ���� | |
| D�� | Cl2��ˮ��Һ�ܹ����磬��Cl2�Ȳ��ǵ����Ҳ���Ƿǵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
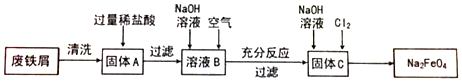
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������������������ | |
| B�� | ��Һ�в�����Fe3+ | |
| C�� | �����������ᣬ����Һ��Fe3+Ũ�Ȼ��С | |
| D�� | ��ϵ�д��������������ij����ܽ�ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����١��۵IJ������ǹ��� | |
| B�� | ���õ�����Һ���鲽��ڵķ�Ӧ�Ƿ������ȫ | |
| C�� | ������м�����л��ܼ����Ҵ� | |
| D�� | ����ܵIJ����Ǿ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
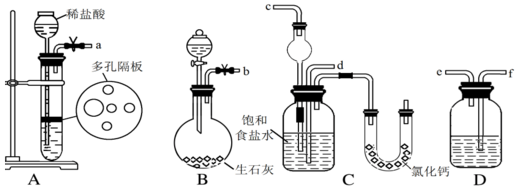
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | m=53��c2=a/b | B�� | m=-26.5��2c=a-b | C�� | m=-170.5��2c=a-b | D�� | m=26.5��c2=$\frac{a}{b}$ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com