
| A. | 石油干馏可得到汽油、煤油等 | |
| B. | 破坏乙烯分子里C=C键所需吸收的能量是破坏乙烷分子里C-C键能量的两倍 | |
| C. | 油脂不是高分子化合物,1mol油脂完全皂化生成1mol甘油和3 mol高级脂肪酸 | |
| D. |  和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物 ,该反应符合绿色化学的原则 ,该反应符合绿色化学的原则 |
分析 A.石油分馏可得到汽油、煤油;
B.C=C双键的键能小于C-C单键键能的2倍;
C.油脂在碱性条件下的水解为皂化反应;
D.该反应过程原子利用率达100%.
解答 解:A.石油分馏可得到汽油、煤油,故A错误;
B.C=C双键的键能小于C-C单键键能的2倍,大于C-C单键键能,故B错误;
C.1mol油脂完全皂化生成1mol甘油和3 mol高级脂肪酸钠,故C错误;
D.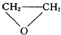 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物 ,该反应过程原子利用率达100%,所以该反应符合绿色化学的原则,故D正确.
,该反应过程原子利用率达100%,所以该反应符合绿色化学的原则,故D正确.
故选D.
点评 本题考查较为综合,多角度考查有机物的组成、结构和性质,为高频考点,侧重于化学与生活的考查,有利于培养学生的良好的科学素养,难度不大.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:解答题
 ),乳酸在微生物作用下分解为CO2和H2O.
),乳酸在微生物作用下分解为CO2和H2O.
 乳酸在一定条件下发生反应得到聚乳酸的化学方程式是n
乳酸在一定条件下发生反应得到聚乳酸的化学方程式是n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +(n-1)H2O.
+(n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| C. | 常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 向AgNO3溶液中通入少量HCl | B. | 向H2SO3溶液中通入Cl2 | ||
| C. | 向FeI2溶液中通入少量Cl2 | D. | 向NaOH溶液中通入少量Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铁溶液保存时加入少量的盐酸 | B. | 氯水保存在棕色瓶里并放在冷暗处 | ||
| C. | 漂白粉可以在敞口容器中长期存放 | D. | 溴水盛放在有玻璃塞的细口瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.4 g | B. | 2.8 g | ||
| C. | 4.4 g | D. | 在1.4 g和2.8 g之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com