
【题目】金属在人类社会发展进程中发挥了重要作用,钠、镁、铝、铁、铜是最重要的几种金属。
(1)上述五种金属中人们发现并最早制得其单质的是_____________。
(2)这五种金属单质都具有的性质是_________________(填下列选项的序号)。
a.导电性 b.延展性 c.银白色 d.熔点高 e.硬度大
(3)钠、镁、铝、铁四种金属中,不能用于从氯化铜溶液中置换出铜的金属是_________,原因是 _________(用必要的化学方程式表示)。
(4)上述金属中,有一种金属的氧化物能在另一种金属的氢氧化物的水溶液中溶解,写出反应的离子方程式:_________________。
【答案】Cu(或铜) ab Na(或钠) 2Na+CuCl2+2H2O=Cu(OH)2↓+ H2↑+2NaCl Al2O3+2OH-=2AlO2-+ H2O
【解析】
(1)不活泼金属最早被使用;
(2)金属的通性为:导电、导热性,良好的延展性,大多数熔点低、硬度小,某些金属略带金属光泽;
(3)钠的性质活泼,先与水反应,不能与盐溶液发生置换反应生成金属单质;
(4)NaOH可溶解氧化铝生成偏铝酸钠和水。
由金属的活泼性可知,上述五种金属中人们发现并最早制得其单质的是Cu(或铜);
故答案为:Cu(或铜);
由金属的通性可知,这五种金属单质都具有的性质是ab;
故答案为:ab;
钠、镁、铝、铁四种金属中,不能用于从氯化铜溶液中置换出铜的金属是Na(或钠),原因是![]() ;
;
故答案为:Na(或钠);![]() ;
;
上述金属中,有一种金属的氧化物能在另一种金属的氢氧化物的水溶液中溶解,反应的离子方程式为![]() ;
;
故答案为:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备Cu2(OH)2CO3,其工艺流程如下:
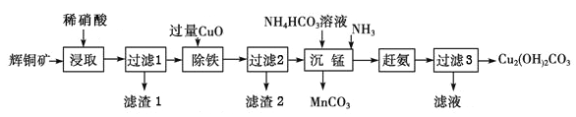
(1)“酸浸”过程中,将矿石粉碎,其目的是__________;加热能加快矿石粉“酸浸”速率,但温度不宜过高,其原因是__________。
(2)Cu2S和硝酸反应,其还原产物为NO。已知1 mol Cu2S完全反应时转移10 mol电子。写出该反应的离子方程式:_____________________。
(3)“除铁”中加入过量氧化铜发生反应的离子方程式为___________________。
(4)从过滤3得到的滤液中可提取一种肥料,它的化学式为__________;滤渣1的主要成分是__________(填化学式)。
(5)设计实验确认过滤2得到的滤液中是否有Fe3+:___________________________。
(6)取wg辉铜矿经上述流程转化,加入agCuO,滤渣2含bgCuO,最终得cmolCu2(OH)2CO3不考虑铜元素损失)。原辉铜矿含Cu2S的质量分数为____________。(用代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废物的处理、转化和利用是非常有意义的。某研究性学习小组设计如图所示流程,综合处理某工厂印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)和废气(H2S),真正做到了变废为宝:处理废液、废气得到氯化铜、单质硫的同时,还实现了蚀刻液的循环利用。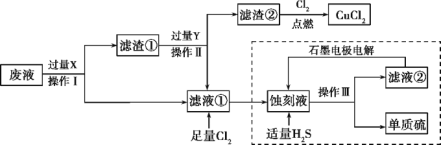
根据以上信息回答下列问题:
(1)操作I、Ⅱ、Ⅲ相同,名称是__,所需要的玻璃仪器主要有:烧杯、玻璃棒、__。
(2)通常用来检验蚀刻液中金属阳离子的化学试剂是__。
(3)向废液中加入过量X时发生的主要反应的离子方程式为__。
(4)滤渣①与Y反应的化学方程式为____。
(5)H2S通入蚀刻液中发生的主要反应为___。
(6)电解池中H+在阴极放电产生H2,阳极的电极反应式为__。
(7)综合分析虚线框内所涉及的两个反应,可知该过程有两个显著优点:①蚀刻液得到循环利用;②__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等离不开化学。
(1)普通玻璃是常见的硅酸盐产品,其主要成分的化学式为Na2CaSi6O14,以氧化物形式可表示为______。
(2)缺铁性贫血患者补充的铁,通常为硫酸亚铁的形式,而硫酸铁则没有这种药效.当用硫酸亚铁制成药片时外表要包有一层特殊的糖衣,这层糖衣的作用是______.若在酸性的硫酸亚铁溶液中通入氧气,也能得到棕黄色溶液,请写出此反应的离子方程式______.检验棕黄色溶液是否有Fe2+,可选用的试剂为______(填字母)。
A.稀硝酸B.浓硫酸C.KSCN溶液D.酸性高锰酸钾溶液
(3)从降低成本和减少环境污染的角度考虑,制取硫酸铜最好的方法是______(填字母)。
A.铜和浓硫酸反应B.铜和稀硫酸反应
C.氧化铜和硫酸反应D.铜与Fe2(SO4)3溶液反应
(4)实验室用硫酸铜晶体配制一定物质的量浓度的硫酸铜溶液,下列操作将使所配溶液物质的量浓度偏高的是______(填字母)。
A.所用的硫酸铜晶体已经部分风化失水
B.移液时不小心溅出少许溶液
C.容量瓶查漏后未经干燥就直接使用
D.定容时俯视容量瓶刻度线
E.未洗涤烧杯和玻璃棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若m g Al在足量氯气中燃烧,生成固体的质量为(m+21.3)g,将m g Al投入总质量为95.2gNaOH水溶液中恰好完全反应。下列判断正确的是( )
A.m=2.7
B.Al与Cl2反应的产物溶于水,所得溶液中加入足量氨水,先出现沉淀,后又溶解
C.若在原NaOH溶液中通入足量Cl2,理论上可生成0.2molNaClO
D.Al与NaOH溶液反应后所得溶液中溶质的质量分数为16.4%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—股淡淡清香能给人心旷神怡的感觉,主要由香精、酒精和水构成的香水备受爱美人士的青睐。香精里面含有酯类物质,工业上以A为主要原料来合成乙酸乙酯,其合成路线如下图所示,其中A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平。又知2CH3CHO+O2![]() 2CH3COOH。请回答下列问题:
2CH3COOH。请回答下列问题:
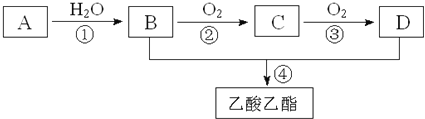
(1)写出A的电子式__________;
(2)B、D分子内含有的官能团分别是__________、__________(填名称);
(3)写出下列反应的反应类型:①______________,④______________;
(4)写出下列反应的化学方程式:
①__________________________________________________;
②__________________________________________________;
④__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中除含有Ca2+、Mg2+、SO42-等可溶性杂质外,还含有泥砂等不溶性杂质。
(1)检验溶液中含有SO42-的方法是_________________。
(2)将粗盐溶解过滤除去不溶性杂质后,在滤液中依次滴加过量NaOH溶液、BaCl2溶液和Na2CO3溶液,直至不再产生沉淀。这些操作的目的是_________________,滴加Na2CO3溶液时发生反应的化学方程式为________________。
(3)用提纯后的NaCl固体配制100mL l.0mol/LNaCl溶液,所用仪器除托盘天平、烧杯、玻璃棒、药匙外,还需要___________(填仪器名称)。转移溶液时没有洗涤烧杯会造成所配溶液浓度偏______(填“高”或“低”,下同),定容时仰视刻度线会造成所配溶液浓度偏____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列是八种环状的烃类物质:
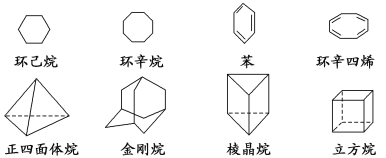
(1)互为同系物的有________和________(填名称)。互为同分异构体的有________和________、______和________……(填写名称,可以不填满,也可以再补充)。
(2)正四面体烷的一氯取代产物有________种,二氯取代产物有________种;立方烷的一氯取代产物有________种,二氯取代产物有________种;金刚烷的一氯取代产物有________种。
Ⅱ.如图所示都是简化的碳骨架结构,请回答:
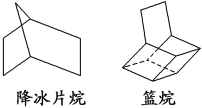
(1)其分子式分别是________、________。
(2)降冰片烷发生一氯取代时,取代位置有______种。
(3)篮烷发生一氯取代时,其一氯取代物有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展,其结构简式为:
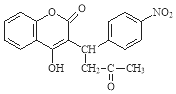
醋硝香豆素可以通过以下方法合成(部分反应条件省略)。

已知: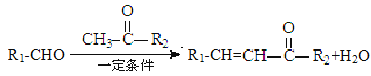
回答以下问题:
(1)反应①的反应类型是______。
(2)从A到B引入的官能团名称是______。
(3)物质C的结构简式为______。
(4)反应③的化学方程式为______。
(5)关于E物质,下列说法正确的是______(填字母序号)。
a 在核磁共振氢谱中有四组吸收峰
b 可以用酸性高锰酸钾溶液鉴别D和E
c 可以发生加成反应、聚合反应、氧化反应和还原反应
d 存在顺反异构
(6)分子结构中只含有一个苯环,且同时符合下列条件的G的同分异构体共有______种。
①可与氯化铁溶液发生显色反应;
②可与碳酸氢钠溶液反应生成二氧化碳气体。其中,苯环上的一氯代物只有两种的同分异构体的结构简式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com