
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 0.5 mol Cu与足量的S反应转移电子数为![]()
B. 在粗铜精炼的实验中,阳极质量减小6.4g,则电解过程中转移电子数为0.2![]()
C. 2 g D2O和H218O的混合物中含有的中子数为![]()
D. 46 g 有机物C2H6O中含有极性共价键的数目一定为7![]()
【答案】C
【解析】
A. Cu与足量的S反应生成硫化亚铜,1mol铜完全反应转移电子数为NA,所以0.5 mol Cu与足量的S反应转移电子数为0.5NA,故A错误;
B.粗铜中含有杂质铁、锌等,所以阳极质量减少6.4g时,电路中转移电子的物质的量不一定为0.2mol,转移电子的数目不一定为0.2 NA,故B错误;
C.2g D2O的物质的量为0.1mol,含有中子数为NA; 2g H 218O的的物质的量为0.1mol,含有中子数为NA;根据极值法可知:2g D2O和H218O的混合物中含有的中子数为NA,故C正确;
D. 46g 有机物C2H6O物质的量为1mol;若C2H6O为乙醇,1mol乙醇含有极性共价键的数目为7NA,若C2H6O为甲醚,1mol二甲醚含有极性共价键的数目为8NA;故D错误;
综上所述,本题选C。


科目:高中化学 来源: 题型:
【题目】下列实验操作或数据记录不正确的是:
A.用10 mL量筒量取9.2 mL NaCl溶液
B.用酸式滴定管量取20.00 mL K2Cr2O7溶液
C.用电子(分析)天平测得铁片质量是15.5240 g
D.用托盘天平称量时,将NaOH固体放在滤纸上,称得质量为4.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO3>I,氧化性IO3> I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法不正确的是

A. 0--b :3HSO3-+ IO3-= 3SO42-+ I-+ 3H+
B. a点时消耗NaHSO3的物质的量为1.2 mol
C. b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2
D. 当溶液中I与I2的物质的量之比为5∶2时,加入的KIO3为1.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:

(1)从上图实验装置看,其中尚缺少的一种玻璃用品是______;
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用________。
(3)若改用60mL0.25mol·L-1H2SO4和50mL0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量________(填“相等”、“不相等”)。
(4)50mL0.55mol/L NaOH溶液和50mL0.25mol/L硫酸溶液的实验数据如下表:
请填写下表中的空白:______

②近似认为50mL0.55mol/LNaOH溶液和50mL0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=______kJ/mol(取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是______。
a.实验装置保温.隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三蝶烯是最初的“分子马达”的关键组件,三碟烯某衍生物X可用于制备吸附材料,其结构如图所示,3个苯环在空间上互为120°夹角。下列有关X的说法正确的是( )
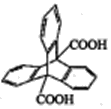
A. 分子式为C22H13O4 B. 1mol该物质与H2加成可消耗11mol H2
C. 苯环上的一氯代物有3种 D. 分子中最多可能有20个原子位于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是( )
3C+4D反应中,表示该反应速率最快的是( )
A. v(A)=0.5mol·L-1·s-1B. v(B)=0.3mol·L-1·s-1
C. v(C)=0.8mol·L-1·s-1D. v(D)=30mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在加热条件下利用二氧化锰与浓盐酸反应来制取并收集氯气。
(1)若要制取纯净干燥的氯气,应使气体依次通过装有_______和_____的洗气瓶。
(2)实验室中若无MnO2,可用固体KMnO4代替,发生下列反应:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O,则可选择的气体发生装置是(填序号)___________。
a. b.
b. c.
c.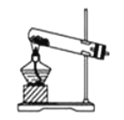
(3)某同学不慎将MnO2和KCl粉末混合了,分离该混合物的方法和步骤如下,请补充完整:先在盛有混合粉末的烧杯中加入适量的水溶解;然后____、洗涤、干燥沉淀得到MnO2;将所得液体________,即得到KCl固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硒![]() 是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓
是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓![]() 或浓
或浓![]() 反应生成
反应生成![]() 以回收
以回收![]() 。涉及如下化学反应:
。涉及如下化学反应:
①![]()
②![]()
③![]()
下列有关叙述正确的是
A. ![]() 、
、![]() (浓)、
(浓)、![]() 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是![]() (浓)>
(浓)>![]() >
>![]()
B. 反应①中![]() 是氧化物,
是氧化物,![]() 是还原产物
是还原产物
C. 反应①中每有0.6 mol ![]() 生成,转移电子数目为2.4
生成,转移电子数目为2.4![]()
D. 反应②③中等量的![]() 消耗浓
消耗浓![]() 和浓
和浓![]() 的物质的量之比为2:1
的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为 2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是 ( )

A. 反应中有0.5 NA个电子转移时,析出0.5molCu2O
B. 正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH-
C. 测量原理示意图中,电子方向从Ag2O→Cu
D. 电池工作时,OH-离子浓度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com