
| A. | 铁与盐酸反应生成氯化铁和氢气 | |
| B. | 铁在高温下与水蒸气的反应是置换反应 | |
| C. | 铁与盐酸、水蒸气反应,均作还原剂 | |
| D. | 铁丝在空气、纯氧中均不能燃烧 |
科目:高中化学 来源: 题型:选择题
| A. | 1molOH-的质量是17g | B. | 1mol气体所占的体积等于22.4L | ||
| C. | 氢气的摩尔质量是2g | D. | 摩尔是物质的质量单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①②③ | C. | ②③④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知:还原性HSO3->I-,氧化性IO3->I2.在含3molNaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图所示.下列说法正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含3molNaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图所示.下列说法正确的是( )| A. | 反应过程中的氧化产物均为Na2HSO4 | |
| B. | a点时剩余NaHSO3的物质的量为1.0 mol | |
| C. | 0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-+3OH-=3SO43-+I-+3H2O | |
| D. | 当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为1.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用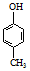 和HCHO 为原料合成 和HCHO 为原料合成 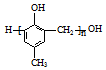 | |
| B. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| C. | C3H8的六氯代物共有4种,而且CH3-CH=CH-CH3与C3H6一定互为同系物 | |
| D. | 将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是还原糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )| A. | a的取值范围为0≤a<50 | |
| B. | 当a=30时,$\frac{n(Mg)}{n(Al)}$=1 | |
| C. | 图中0~a段,与NaOH发生反应的微粒是H+ | |
| D. | 当v(NaOH)=90mL时,溶液中的溶质为NaAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
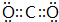 ,BA2分子中化学键属于共价键.
,BA2分子中化学键属于共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用100mL量筒量取5.2mL的稀硫酸 | |
| B. | 用500mL容量瓶配制480mL 0.2mol/L的NaOH溶液 | |
| C. | 用托盘天平称量11.75克NaCl晶体 | |
| D. | 用分液漏斗进行固体和液体的分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 苯酚能跟NaOH溶液反应,而乙醇不能与NaOH溶液反应 | |
| C. | 苯与硝酸在加热的条件生成硝基苯,而甲苯在加热条件下与硝酸发生反应生成三硝基甲苯 | |
| D. | 乙炔能发生加成,乙烷不能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com