
【题目】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业,是难溶于水的白色固体,能溶解于硝酸,在潮湿空气中可被迅速氧化。
Ⅰ.实验室用CuSO4—NaCl混合液与Na2SO3溶液反应制取CuCl。相关装置及数据如图。
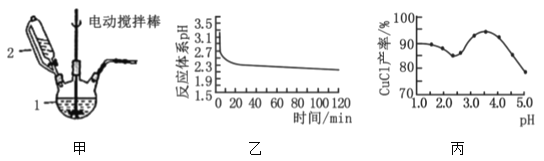
回答以下问题:
(1)甲图中仪器1的名称是___;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3-,为提高产率,仪器2中所加试剂应为___。
(2)乙图是体系pH随时间变化关系图,写出制备CuCl的离子方程式___。丙图是产率随pH变化关系图,实验过程中往往用Na2SO3—Na2CO3混合溶液代替Na2SO3溶液,其中Na2SO3的作用是___并维持pH在___左右以保证较高产率。
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是___。
Ⅱ.工业上常用CuCl作O2、CO的吸收剂,某同学利用如图所示装置模拟工业上测定高炉煤气中CO、CO2、N2和O2的含量。
A. | B. |
C. | D. |
已知:Na2S2O4和KOH的混合溶液可吸收氧气。
(4)装置A中用盐酸而不能用硝酸,其原因是___(用化学方程式表示)。用D装置测N2含量,读数时应注意___。整套实验装置的连接顺序应为___→D。
【答案】三颈烧瓶 Na2SO3溶液 2Cu2++SO32-+2Cl-+H2O=2CuCl↓+2H++SO42- 与H+作用,调整pH 3.5 洗去晶体表面的杂质离子,同时防止CuCl被氧化 6CuCl+8HNO3=3Cu(NO3)2+3CuCl2+2NO↑+4H2O(或3CuCl+7HNO3=3Cu(NO3)2+3HCl+NO↑+2H2O) 温度降到常温,上下调节量气管至左、右液面相平,该数时视线与凹液面最低处相切 C→B→A
【解析】
(1)根据仪器1的图示解答;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3- ,需要控制Na2SO3的加入量,据此分析判断;
(2)根据题意,在CuSO4液中加入一定量的Na2SO3和NaCl溶液生成CuCl沉淀,同时溶液的酸性增强,结合Na2CO3的性质分析解答;
(3)根据“氯化亚铜(CuCl)在潮湿空气中可被迅速氧化”分析解答;
(4)根据氯化亚铜(CuCl)能溶解于硝酸 ,结合硝酸的强氧化性书写反应的方程式;根据正确的读数方法解答;用CuCl作O2、CO的吸收剂,测定高炉煤气中CO、CO2、N2和O2的含量,可用KOH吸收二氧化碳,然后用B吸收氧气,再用A吸收CO ,最后用排水法测量氮气的体积,据此分析解答。
(1)甲图中仪器1为三颈烧瓶;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3- ,为提高产率,可控制Na2SO3的加入量,则仪器2中所加试剂应为Na2SO3溶液;
(2)在提纯后的CuSO4液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl(氯化亚铜)沉淀,同时溶液的酸性增强,生成硫酸,反应的离子方程式为: 2Cu2++SO32-+2Cl-+H2O=2CuCl↓+2H++SO42-,用Na2SO3-Na2CO3混合溶液代替Na2SO3溶液,Na2CO3可与生成的H+反应,及时除去系统中反应生成的H+,利于反应进行,由图象可知,应维持pH在3.5左右;
(3)用去氧水作洗涤剂洗涤产品,可洗去晶体表面的杂质离子,同时防止CuCl被氧化;
(4)根据题意,氯化亚铜(CuCl)能溶解于硝酸,反应的方程式为6CuCl+8HNO3=3Cu(NO3)2+3CuCl2+2NO↑+4H2O(或3CuCl+7HNO3=3Cu(NO3)2+3HCl+NO↑+2H2O);用D装置测N2含量,应注意温度在常温,且左右液面相平,读数时视线与凹液面最低处水平相切,以减小实验误差;用CuCl作O2、CO的吸收剂,测定高炉煤气中CO、CO2、 N2和O2的含量,可用KOH吸收二氧化碳,然后用B吸收氧气,再用A吸收CO,最后用排水法测量氮气的体积,则顺序为C-B-A-D。


科目:高中化学 来源: 题型:
【题目】2018年国际计量大会将“摩尔”的定义修改为:1摩尔包含6.02214076×1023个基本单元,这一常数被称为阿伏加德罗常数(NA),通常用6.02×1023 mol-1表示,新定义于2019年5月20日正式生效。下列说法不正确的是
A.标准状况下,22.4L的NH3约含有10×6.02×1023个质子
B.由新定义可知,阿伏加德罗常数表达为NA=6.02214076×1023 mol-1
C.标准状况下,18gH2O中约含有1×6.02×1023个氧原子
D.白磷分子(P4)呈正四面体结构,62g白磷中约含有12×6.02×1023个P-P键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用甲苯合成苯甲醛:
 ,
,
下列说法正确的是
A. 甲苯分子中所有原子都在同一平面内 B. 反应①②③的反应类型相同
C. 一氯甲苯的同分异构体有3种 D. 苯甲醇可与金属钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院科学家设计出一套利用SO2和太阳能综合制氢方案,其基本工作原理如图所示。下列说法错误的是
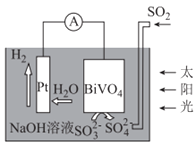
A.该电化学装置中,Pt电极作正极
B.Pt电极的电势高于BiVO4电极的电势
C.电子流向:Pt电极→导线→BiVO4电极→电解质溶液→Pt电极
D.BiVO4电极上的反应式为SO32--2e-+2OH-=SO42-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近一个科学硏究小组创建了一种通过连续电解将能量储存为化学能的装置。在氧化钇基质的阳极和二氧化钛涂覆的钛阴极之间是可通过H+的固体聚合物电解质。其结构如图所示,则下列说法正确的是
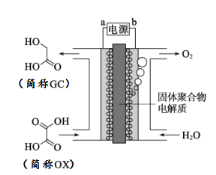
A. 电源的b极为负极
B. 在能量转换过程中,固体电解质中H+由阴极向阳极移动
C. 阴极电极反应式为:OX + 4H+ + 4e﹣═ GC + H2O
D. 为增强阳极电解液导电性,可在水中添加适量NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BHT是一种常用的食品抗氧化剂。由对甲基苯酚(![]() )合成BHT的常用方法有2种(如图)。下列说法中,不正确的是
)合成BHT的常用方法有2种(如图)。下列说法中,不正确的是
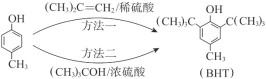
A. BHT能使酸性KMnO4溶液褪色
B. BHT与对甲基苯酚互为同系物
C. BHT与FeCl3溶液不发生显色反应
D. 方法一的原子利用率高于方法二
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图所示的有机物X可生产S—诱抗素Y。下列说法正确的是( )

A.X和Y都可以与FeCl3溶液发生显色反应
B.1 mol Y最多能加成3 mol H2
C.l mol X与足量NaOH溶液反应,最多消耗6 mol NaOH
D.X到Y的反应是水解反应或取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表共有18个纵行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列。按这种规定,下面说法正确的是( )
A. 最外层电子数为ns2的元素都在第2列
B. 第5列元素的原子最外层电子的排布式为![]()
C. 第10、11列为ds区的元素
D. 形成化合物种类最多的元素在第14列,属于P区的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“西气东输”是西部开发的重点工程,这里的“气”是指天然气,其主要成分是甲烷。
(1)甲烷分子具有________________结构,其结构式是_________________。
(2)通常情况下,甲烷比较稳定,但在特定条件下,甲烷也会发生某些反应,请写出甲烷在光照条件下与氯气反应生成一氯甲烷的化学方程式________________________,该反应属于____________(填反应类型)。
(3)在一定条件下甲烷也可用于燃料电池。如图是甲烷燃料电池的原理示意图:
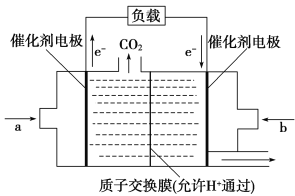
若正极的反应式为O2+4H++4e-=2H2O,则负极反应式为________________________________;该电池工作过程中,H+的移动方向为从________到________(填“左”或“右”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com