
| A. | “血液透析”利用了胶体的性质 | |
| B. | 竹炭具有超强的吸附能力,能吸附新装修房屋内的有害气体 | |
| C. | 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| D. | 海水淡化可以解决淡水危机,向海水中加入明矾可以使海水淡化 |
分析 A、人体血液属于胶体,不能透过半透膜;
B、竹炭具有吸附性,可用于吸附房屋装修产生的有害气体;
C、碳酸氢钠能和酸反应放出气体还没有腐蚀性,不会对人体造成伤害;
D、明矾只能作为净水剂,但不能使海水淡化.
解答 解:A、透析是通过小分子经过半透膜扩散到水(或缓冲液)的原理,将小分子与生物大分子分开的一种分离技术,人体的血液属于胶体,不能透过半透膜,故A正确;
B、竹炭具有超强的吸附能力,能吸附新装修房屋内的有害气体,故B正确;
C、碳酸氢钠和酸反应能生成二氧化碳,可用来发酵,也可治疗胃酸过多,故C正确;
D、明矾溶于水生成氢氧化铝胶体能吸附水中的悬浮颗粒,但不能除去海水中的盐分使海水淡化,故D错误;
故选D.
点评 本题考查化学与生活、生产密切相关的知识,题目难度不大,学习中注意竹炭的应用、胶体的性质、明矾净水原理是解答的关键.


科目:高中化学 来源: 题型:解答题
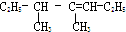 4,5-二甲基-3-庚烯
4,5-二甲基-3-庚烯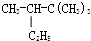 2,2,3一三甲基戊烷
2,2,3一三甲基戊烷查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ①②④⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 制备水杨酸对正辛基苯基酯(
制备水杨酸对正辛基苯基酯( )如下:
)如下:
 ],温度控制在100℃左右,不断搅拌.
],温度控制在100℃左右,不断搅拌. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).
有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的原子序数A>B>C | B. | 它们的离子半径A2->C->B2+ | ||
| C. | 它们的原子半径C>B>A | D. | 它们的最外层电子数C>A>B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com