
【题目】常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。下列叙述正确的是( ) 
A.所用盐酸的浓度是0.09mol·L─1 , NaOH溶液浓度为0.03mol·L─1
B.在B点,溶液中离子浓度关系为:c(Cl─)>c(Na+)>c(OH-)>c(H+)
C.A,B,C三点水的电离程度大小依次为:A>B>C
D.滴定前,锥形瓶用待测液润洗,导致盐酸浓度偏低
【答案】A
【解析】结合图像,假设HCl的浓度是x mol·L─1 , NaOH溶液浓度为y mol·L─1 , 有:20×10─3×x=60×10─3×y , ─lg( 20×10─3×x─40×10─3×y(20+40 )=2;解得:x=0.09,y=0.03,A项正确;B点,溶液显酸性, c(H+)>c(OH_),B项错误;A、B、C三点酸性依次减弱,水电离程度逐渐增大,C项错误;滴定前,锥形瓶用待测液润洗,增加n(H+),消耗n(NaOH)增大,导致盐酸浓度偏高,D项错误。
【考点精析】本题主要考查了酸碱中和滴定的相关知识点,需要掌握中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】对乙酰氨基苯酚M( ![]() )是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下:
)是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下: 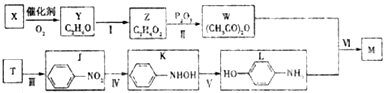
已知:①X,Y,T分子的核碰共振氢谱只显示1组峰,且X能使溴水褪色;
② ![]() .
.
(1)X,Y的结构简式为、;
(2)Ⅲ的反应类型为 , Ⅵ的反应方程式为;
(3)M与足量氢氧化钠溶液反应的化学方程式为;
(4)M有多种同分异构体,其中一类与J互为同系物且氮原子与苯环直接相连,此类同分异构体共有种; 另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有﹣NH2;②能发生水解反应;③核碰共振氢谱有4组峰.写出其中一种同分异构体的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每一方框中的字母代表一种反应物或生成物:
物质A跟B反应生成物质E、F和G;物质C跟D反应生成物质I,其中B是一种黄氯色气体,C是一种可燃性气体,D气体是空气的主要成分之一,I的水溶液显碱性.请填写下列空白: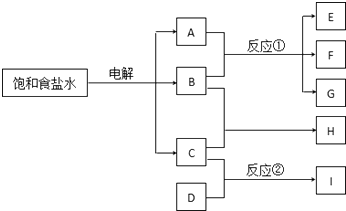
(1)物质H的化学式是 .
(2)写出电解饱和食盐水的反应方程式:
(3)分别写出电解过程中产生B、C气体的电极反应式:、
(4)反应①的化学方程式是 .
(5)反应②的化学方程式(应注明反应条件)是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室中进行如下实验:
编号 | Ⅰ | Ⅱ | Ⅲ |
实验 |
|
|
|
现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
以下结论正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为CuCl2
C.Ⅲ中的离子方程式为2H++Zn═Zn2++H2↑
D.Ⅲ中发生的反应不是离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空
(1)有机物 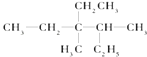 用系统命名法命名:
用系统命名法命名:
(2)写出4甲基2乙基1戊烯的结构简式:
(3)某烃的结构简式是 ![]() ,分子中饱和碳原子数为 , 可能在同一平面上的碳原子数最多为
,分子中饱和碳原子数为 , 可能在同一平面上的碳原子数最多为
(4)下列物质中属于同系物的是
①CH3CH2Cl②CH2═CHCl ③CH3CH2CH2Cl④CH2ClCH2Cl⑤CH3CH2CH2CH3 ⑥CH3CH(CH3)2
A.①②
B.①④
C.①③
D.⑤⑥
(5)0.1mol某烷烃燃烧,其燃烧产物全部被碱石灰吸收,碱石灰增39g.该烃的分子式为;若它的核磁共振氢谱共有3个峰,则该烃可能的结构简式为 . (写出其中一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物6.4g在O2中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确的是( )
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1:2
C.无法确定该化合物是否含有氧元素
D.该化合物中一定含有氧元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用包括很多方面,下图是从海水中通过一系列工艺流程提取产品的流程图。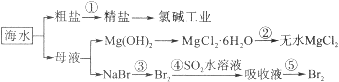
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子。
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。回答下列问题:
(1)海水pH约为8的原因主要是天然海水含上述离子中的。
(2)除去粗盐溶液中的杂质(Mg2+、SO42-、Ca2+),加入药品的顺序可以为。
①NaOH溶液 ②BaCl2溶液 ③过滤后加盐酸 ④Na2CO3溶液
(3)过程②中由MgCl2·6H2O制得无水MgCl2 , 应如何操作。
(4)从能量角度来看,氯碱工业中的电解饱和食盐水是一个将转化为的过程。采用石墨阳极,不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式。
(5)从第③步到第④步的目的是。采用“空气吹出法”从浓海水中吹出Br2 , 并用SO2吸收。主要反应的化学方程式为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com