
【题目】已知![]() 为
为![]() 和
和![]() 的混合物,且知氧化性顺序:
的混合物,且知氧化性顺序:![]() ,取
,取![]() 样品进行如下图所示的实验:
样品进行如下图所示的实验:
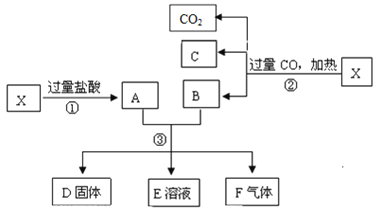
(1)写出③步可能发生反应的3个离子方程式为________________________、________________________、________________________。
(2)若溶液E中只有一种金属离子,则一定是______;若D固体是纯净物,该固体是______。(填化学式)
(3)向溶液A中加入![]() 粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________。
粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________。
【答案】Cu2++Fe═Fe2++Cu 2Fe3++Fe═3Fe2+ 2Fe3++Cu=Cu2++2Fe2+ Fe2+ Cu 2Fe3++Cu=Cu2++2Fe2+
【解析】
(1)X为Fe2O3和CuO的混合物,与过量盐酸反应生成的A中含有氯化铁、氯化铜和盐酸,Fe2O3和CuO的混合物被一氧化碳还原后可得到的固体有铜、铁两种,若B是铜,根据氧化性顺序可知,只有一个反应:2Fe3++Cu=2Fe2++Cu2+,且不会产生F气体,故B是铁和铜,据此分析;
(2)若溶液E中只有一种金属离子,则必然是氧化性最弱的离子;由于铜的还原性小于铁的还原性,Fe首先还原Fe3+,然后再还原Cu2+,所以D固体如果是纯净物,则一定是Cu;
(3)由于氧化性Fe3+>Cu2+,Fe3+能氧化Cu,据此分析。
(1)X为Fe2O3和CuO的混合物,与盐酸反应生成的A中含有氯化铁和氯化铜,被一氧化碳还原后生成的B中含有铜和铁的单质,由于氧化性Fe3+>Cu2+>H+>Fe2+,所以溶液中可能发生的离子反应有:Cu2++Fe═Fe2++Cu、2Fe3++Fe═3Fe2+、2Fe3++Cu=Cu2++2Fe2+,
(2)根据(1)中发生的离子反应可知,溶液中一定有Fe2+;由于铜的还原性小于铁的还原性,故Fe首先还原Fe3+,该过程无固体析出,然后再还原Cu2+,生成Cu,所以D固体如果是纯净物,则一定是Cu;
(3)由(1)分析可知,A溶液中一定含有Fe3+,根据氧化强弱可知,Fe3+可以氧化Cu,生成Cu2+,离子反应方程式为2Fe3++Cu=Cu2++2Fe2+。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,五种含有同种金属元素的单质或其化合物,能按如图箭头方向实现一步转化(不含电解),该金属元素可能是( )
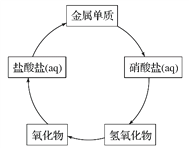
①Fe ②Cu ③Al ④Na
A. ①② B. ②④
C. ①③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物在冬季来临过程中,随着气温的逐渐降低,体内发生了一系列适应低温的生理生化变化,抗寒力逐渐增强。下图为冬小麦在不同时期含水量和呼吸速率变化关系图。请根据图推断以下有关说法中,错误的是( )

A. 冬季来临过程中,自由水明显减少是呼吸速率下降的主要原因
B. 结合水与自由水含量的比值,与植物的抗寒性呈现明显的正相关
C. 随着气温和土壤温度的下降,根系的吸水量减少,组织的含水量下降
D. 随温度的缓慢降低,植物的呼吸作用逐渐减弱,有利于减少有机物的消耗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一份含有杂质MgCl2和KCl的AlCl3溶液M,某小组用下图所示过程对其进行除杂并尽可能的减少AlCl3的损失。请回答下列问题:
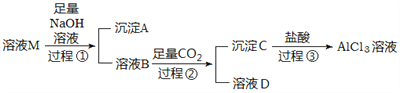
(1)沉淀A的化学式为__________,过程①中Al3+发生反应的离子方程式为__________________。
(2)氢氧化钠溶液_____(填“能”或“不能”)用氨水代替,原因是_____________________。
(3)溶液B中大量存在的阳离子是______________,过程②中生成沉淀C的离子方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向KOH溶液中通入11.2L(已换算成标准状况下)氯气恰好完全反应生成二种含氯盐:0.7molKC1、0.2mnolKClO和X。则X是
A. 0.1molKClO3 B. 0.2molKClO3 C. 0.1molKClO4 D. 0.2molKClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙是一种温和的氧化剂,常温下为白色固体,易溶于酸,难溶于水、乙醇等溶剂。
(1)某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙,按气流方向连接顺序为__________________(填仪器接口的字母编号,装置可重复使用);实验步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞,通入一段时间气体,加热药品;③反应结束后,先想灭酒精灯,待反应管冷却至室温后,停止通入气体;④拆除装置,取出产物。实验步骤③的操作目的是______________________。
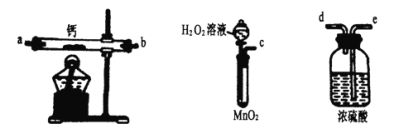
(2)利用反应Ca2++H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4+,在碱性环境下制取CaO2·8H2O的装置如下:

①仪器C的名称____________;反应结束后,经__________(填操作名称)、洗涤、低温烘干可获得CaO2·8H2O。
②装置A中发生反应的化学方程式为_____________;装置B中用冰水浴控制温度,其可能原因是______________________________。
③测定产品中CaO2·8H2O的含量的实验步骤如下:
步骤一:准确称取a g产品放入锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴___________(作指示剂)。
步骤三:逐滴加入浓度为c mol/L的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2次,得出三次平均消耗Na2S2O3溶液体枳为VmL。则CaO2·8H2O的质量分数为____(用含字母的式子表示)。 [已知:I2+2S2O32-=2I-+ S4O62-]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨作为重要化工原料,被大量应用于工业生产。氨在不同催化剂条件下可发生下列两个反应:
反应I:4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g) △H=-905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=-905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1
2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1
(1)写出NO分解生成N2与O2的热化学方程式:___________________________。
(2)反应I在容积固定的密闭容器中进行,容器内部分物质的物质的量浓度如下表:
时间 浓度 | c(NH3)/mol/Ll | c((O2)/mol/L | c(NO)/ mol/L |
第 0 min | 0.8 | 1.6 | 0 |
第 2 min | 0.3 | 0.975 | 0.5 |
第 3 niin | 0.3 | 0.975 | 0.5 |
第4 min | 0.7 | 1.475 | 0.1 |
①反应从开始到第2min时,v(H2O)=__________________。
②在第3min时,改变的反应条件可能是_________(填选项字母)。
A.使用催化剂 B.臧小压强 C.升高温度 D.增加O2的浓度
③该反应达到平衡状态的标志是___________(填选项字母)。
A.在恒温恒容的容器中,混合气体的密度不再变化
B.单位时间内消耗nmolNO的同时消耗nmolNH3
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
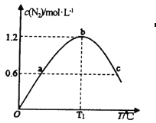
(3)①若在容积为2L的密闭容器中充入8molNH3(g)和6molO2(g),发生反应II。保持其他条件不变,在相同时间内测得c(N2)与温度的关系如图所示。则T1℃下,NH3的平衡转化率为___。
②图中a、c两点对应的容器内部压强Pa____Pc(填“>”、“<”或“=”)
(4)氨气可用于生成硝酸铵化肥。25℃时,已知NH3·H2O的电离常数Kb=1.8×10-5,则硝酸铵在此温度下发生水解反应的平衡常数Kh=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铵可用作肥料,也可用于纺织、皮革、医药等方面。某化学兴趣小组对硫酸铵的一些性质进行探究。回答下列问题:
(1)在试管中加入少量硫酸铵样品,加水溶解,滴加NaOH溶液。将湿润的红色石蕊试纸放在试管口,试纸颜色无明显变化。再将试管加热,试纸很快变蓝。由此可知:______________________________________、_________________________________。
(2)从废铁屑中回收铁屑,用碱溶液洗净之后,再用过量硫酸溶解。然后加入稍过量硫酸铵饱和溶液。在小火下蒸发溶剂直到晶膜出现,停火利用余热蒸发溶剂。过滤后用少量乙醇洗涤,得到硫酸亚铁铵晶体。
①碱溶液洗涤的目的是__________________________________。
②硫酸过量的原因是___________________________________。
(3)硫酸铵高温下完全分解生成氨气和其他几种气体(含硫产物只有一种)。为探究硫酸铵的其他分解产物,通过下列装置进行实验,通入分解产物一段时间后,再点燃装置E中的酒精灯并开始用装置F收集气体。实验中观察到E中无明显现象,F中排水收集的气体能使燃着的木条熄灭,经测定其相对分子质量为28。
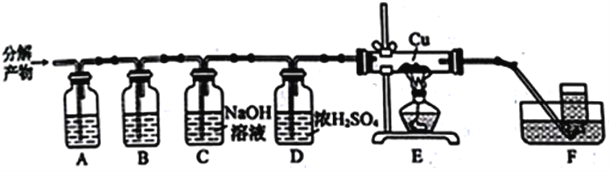
①装置A、B中的溶液分别是______(填标号)。B中可观察到的现象是_____________________。
a.NaOH溶液 b.硫酸溶液 c.BaCl2溶液 d.品红溶液
②装置E的作用是__________________________________。
③写出(NH4)2SO4高温分解的化学方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】认真观察下列有机化合物,回答下列问题:

(1)D中含有的官能团有_________(填写名称,下同),E中含有的官能团有_________________。
(2)下列说法中,错误的是_______。
A.A物质属于酚类 B.B物质分子中含有羧基、醇羟基和酚羟基三种官能团
C.C物质的分子式为C8H8O4 D.F分子中只含有酯基一种官能团
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com