
| m-n | 0 | 1 | 2 | 3 |
| 含氧酸强度 | 弱酸 | 中强 | 强 | 很强 |
| 实例 | HClO | H3PO4 | HNO3 | HClO4 |
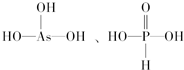 ;
;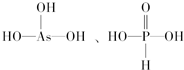 ;
;

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、NH4Cl溶液可用于去除铁锈 |
| B、用硫酸清洗锅中的水垢(主要成分为Mg(OH)2和CaCO3) |
| C、将直径为10-9~10-7m的颗粒均匀分散于水中形成的体系具有丁达尔现象 |
| D、实验室从海带中提取碘的方法是:取样→灼烧→溶解→过滤→氧化→萃取→… |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)2溶液中加入HNO3溶液:Fe(OH)2+2H+═2H2O+Fe2+ |
| B、盐酸除去铜器表面的铜绿:Cu2(OH)2CO3+4H+═3H2O+2Cu2++CO2↑ |
| C、氯气可以降低的SO2的漂白性:SO2+Cl2+2H2O═2Cl-+4H++SO42- |
| D、CO2通入饱和碳酸钠溶液:CO2+CO32-+2Na++H2O═2NaHCO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8g | B、16g |
| C、32g | D、64g |
查看答案和解析>>
科目:高中化学 来源: 题型:
 反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A、A、C两点的反应速率:A>C |
| B、A、C两点气体的颜色:A深,C浅 |
| C、由状态B到状态A,可以用加热的方法 |
| D、A、C两点气体的转化率:A>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是短周期元素组成的非金属单质A、B、C、D,其中B、C、D在常温常压下是气体,其化合物的转化关系图(有关反应的条件及生成的H2O已略去),E是形成酸雨的污染物之一,F是常见的四原子10电子分子,化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.化合物J由两种元素组成,其相对分子质量为32.
如图是短周期元素组成的非金属单质A、B、C、D,其中B、C、D在常温常压下是气体,其化合物的转化关系图(有关反应的条件及生成的H2O已略去),E是形成酸雨的污染物之一,F是常见的四原子10电子分子,化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.化合物J由两种元素组成,其相对分子质量为32.查看答案和解析>>
科目:高中化学 来源: 题型:
| 项目 | pH | Ca2+、Mg2+总浓度 | 细菌个数 |
| 相关值 | 6.5~8.5 | <0.0045mol?L-1 | <100个?mL-1 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com