
【题目】下列关于四个实验装置的说法中正确的是( )


A. 图一:引发铝热反应的操作是点燃镁条
B. 图二:海水淡化的蒸馏操作中缺少了温度计
C. 图三:滴加K3[Fe(CN)6]溶液,产生特征蓝色沉淀
D. 图四:酸式滴定管注入Na2CO3溶液之前应检查是否漏液
【答案】A
【解析】A. 铝热反应的引发就是点燃镁条;B蒸馏操作需要温度计,通过控制蒸气温度来判断蒸出物,但海水淡化不需要温度计,只要收集蒸气即可;C.该装置为原电池,锌活泼作负极,H+作氧化剂在铁电极上放电,故原电池开始工作后铁电极不参加反应,加K3[Fe(CN)6]溶液不会产生特征蓝色沉淀;D项,碳酸钠溶液呈碱性不能注入酸式滴定管。
详解:A.点燃Mg条,引发反应,可引发铝热反应,所以A选项是正确的;
B. 蒸馏操作需要温度计,通过控制蒸气温度来判断蒸出物,但海水淡化不需要温度计,只要收集蒸气即可,故B错误;
C. 该装置为原电池,锌活泼作负极,H+作氧化剂在铁电极上放电,故原电池开始工作后铁电极不参加反应,加K3[Fe(CN)6]溶液不会产生特征蓝色沉淀,故C错误;
D. 碳酸钠溶液呈碱性不能注入酸式滴定管,故D错误。
所以A选项是正确的。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构
B. P4和CH4都是正四面体分子且键角都为109°28′
C. 水分子很稳定与水分子内有氢键有关
D. 晶体熔点由高到低:MgO> H2O > NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分
族 周期 | |||||||
① | |||||||
Li | C | ④ | ⑤ | ⑥ | |||
⑦ | ⑧ | ⑨ | ⑩ | ||||
K | ⑾ | ||||||
(1)表中元素______的非金属性最强(填写元素符号,下同);元素______的单质室温下呈液态,它的原子序数是__________
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有的相同的化学键是________键(填写“离子键”、“极性共价键”或“非极性共价键”);表中元素⑥⑩⑾氢化物的稳定性由大到小的顺序为:____________________(填写化学式,下同;
(3)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是____________;用电子式表示表中⑧⑩两元素形成化合物的过程____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 向氯化铝溶液中加入过量的氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
B. 向次氯酸钙溶液中通入过量的二氧化硫:ClO-+SO2+H2O===HSO![]() +HClO
+HClO
C. NH4HCO3溶液与足量NaOH溶液混合后加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
D. 向Fe(OH)2中加入稀硝酸:3Fe2++4H++NO![]() ===3Fe3++NO↑+2H2O
===3Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中发生如下可逆反应:2X(g)+Y(s)![]() 3Z(g) ΔH= QkJ/mol,下列说法正确的是
3Z(g) ΔH= QkJ/mol,下列说法正确的是
A. 消耗2 mol X同时生成3 mol Z,说明达到了平衡状态
B. 加入少量的Y正反应速率加快
C. 气体的密度不变时,说明达到了平衡状态
D. 加入少量的X,Q变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温、同压下,已知下列各反应为放热反应,下列各热化学方程式中反应热最小的是
A.H2(l)+F2(l)===2HF(g) ΔH1
B.H2(g)+F2(g)===2HF(g) ΔH2
C.H2(g)+F2(g)===2HF(l) ΔH3
D.H2(l)+F2(l)===2HF(l) ΔH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。某化学小组模拟该方法回收铜和制取胆矾,流程简图如下:
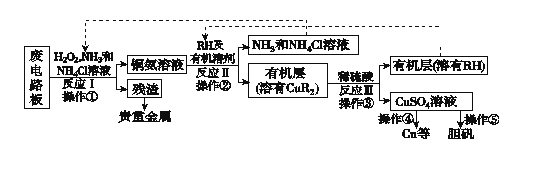
回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH3)42+,反应中H2O2的作用是____________。写出操作①的名称:________。
(2)反应Ⅱ是铜氨溶液中的Cu(NH3)42+与有机物RH反应,写出该反应的离子方程式:__________________________________________。操作②用到的主要仪器名称为______________,其目的是(填序号)________。
a.富集铜元素
b.使铜元素与水溶液中的物质分离
c.增加Cu2+在水中的溶解度
(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和________。若操作③使用如图装置,图中存在的错误是__________________________________________。

(4)操作④以石墨作电极电解CuSO4溶液。阴极析出铜,阳极产物是________________。 流程中有三处实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是实验室制取O2的几种方法:①2KClO3![]() 2KCl+3O2↑;②2H2O2
2KCl+3O2↑;②2H2O2![]() 2H2O+O2↑;③2KMnO4
2H2O+O2↑;③2KMnO4![]() K2MnO4+MnO2+O2↑,则
K2MnO4+MnO2+O2↑,则
A. ①中,MnO2是反应的催化剂
B. ①中,反应前后MnO2化学性质没有改变
C. ②中,反应前后MnO2化学性质发生改变
D. ③中,KMnO4既作氧化剂又作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某学习小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验).
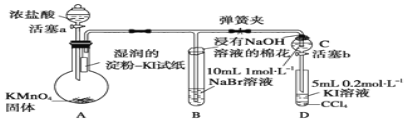
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.
(1)A中产生黄绿色气体,其电子式是 ______;A中使用KMnO4可以在不加热的情况下与浓盐酸发生反应。如果改用二氧化锰,则在加热条件下发生的化学反应方程式为______。
(2)验证氯气的氧化性强于碘的实验现象是 ______ 。
(3)B中溶液发生反应的离子方程式是 ______ 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 ______。
(5)过程Ⅲ实验的目的是 ______ 。
(6)实验结论:氯、溴、碘单质的氧化性逐渐 ______ ,原因是:同主族元素从上到下 ______ ,得电子能力逐渐 ______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com