
【题目】一定条件下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g),请填写下列空白:
xC(g),请填写下列空白:
(1)反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为_____________;x为_______________。
(2)若反应经2min达到平衡,平衡时C的浓度_______0.8mol/L(填“大于,小于或等于”)。
(3)若已知达平衡时,该容器内混合气体总压强为P,混合气体起始压强为P0。请用P0、P来表示达平衡时反应物A的转化率α(A)为_______________%。
(4)能够说明该反应达到平衡的标志是_____________。
A.容器内混合气体的密度保持不变B.υ(A)=3υ(B)
C.A、B的浓度之比为3:1 D.单位时间内消耗3n molA的同时生成n molB
E.体系的温度不再变化
【答案】0.2mol/(Lmin) 2 小于 ![]() DE
DE
【解析】
(1)利用转化物质的量之比等于化学计量数之比计算变化的B的量,结合υ(B)=![]() 计算,利用转化物质的量之比等于化学计量数之比根据x的值;
计算,利用转化物质的量之比等于化学计量数之比根据x的值;
(2)根据随着反应的进行反应物的浓度减少,反应速率减慢,据此判断;
(3)相同条件下,压强之比等于物质的量之比,据此计算平衡后混合气体总的物质的量,利用差量法计算参加反应的A的物质的量,再根据转化率定义计算。
(4)根据平衡状态时物质的浓度不变、物质的含量不变及同一物质表示的正、逆反应速率相等判断平衡状态。
(1)反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,由于反应开始时A的物质的量是3mol,则参加反应的A的物质的量△n(A)=3mol-1.8mol=1.2mol,由于参加反应的物质的量之比等于化学计量数之比,则参加反应的B的物质的量△n(B)=1.2mol×![]() =0.4mol,υ(B)=
=0.4mol,υ(B)=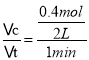 =0.2mol/(Lmin),生成的C的物质的量n(C)=0.4mol/L×2L=0.8mol,由方程式可知,A、C变化的物质的量的比=1.2mol:0.8mol=3:x,解得x=2;
=0.2mol/(Lmin),生成的C的物质的量n(C)=0.4mol/L×2L=0.8mol,由方程式可知,A、C变化的物质的量的比=1.2mol:0.8mol=3:x,解得x=2;
(2)随着反应的进行,物质的浓度逐渐降低,反应速率逐渐减小,若反应经2min达到平衡,后1min的平均速率小于前1min的平均速率,前1min内C的浓度变化为0.4mol/L,则后1min内C的浓度变化小于0.4mol/L,故平衡时C的浓度小于0.8mol/L;
(3)若已知达平衡时,该容器内混合气体总压强为P,混合气体起始压强为P0,则平衡后混合气体总的物质的量n(平衡)=(3mol+1mol)×![]() mol,故平衡后混合气体物质的量减少量为(4-
mol,故平衡后混合气体物质的量减少量为(4-![]() )mol,则根据反应方程式:
)mol,则根据反应方程式:
3A(g)+B(g)![]() 2C(g) 物质的量减少△n
2C(g) 物质的量减少△n
3 2
n(A) (4-![]() )mol
)mol
故n(A)= (4-![]() )mol×
)mol×![]() = (6-
= (6-![]() )mol,所以A物质的转化率为
)mol,所以A物质的转化率为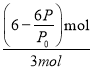 ×100%=
×100%=![]() %。
%。
(4) A.由于反应混合物都是气体,容器的容积不变,因此任何条件下气体的密度都不变,故不能根据容器内混合气体的密度保持不变判断平衡状态,A错误;
B.在任何条件下用A、B表示的反应速率都符合关系υ(A)=3υ(B) ,所以不能确定反应是否达到平衡状态,B错误;
C.A、B两种物质加入的物质的量的比是3:1,消耗的物质的量的比是3:1,因此无论反应是否达到平衡状态,A、B的浓度之比总为3:1,不能据此判断是否为平衡状态,C错误;
D.单位时间内消耗3n molA,就会消耗nmolB,同时生成n molB,说明B的浓度不变,反应达到平衡状态,D正确;
E.任何反应过程中都有化学键的断裂和形成,因此都会有能量发生变化,若体系的温度不再变化,说明反应达到平衡状态,E正确;
故合理选项是DE。


科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | C2H5OH(H2O) | Na | 蒸馏 |
B | CH4(C2H4) | 溴水 | 洗气 |
C | 苯(苯酚) | 浓溴水 | 过滤 |
D | 甲苯(苯) | 酸性高锰酸钾溶液 | 分液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学反应方程式(注明反应条件)并指出反应类型
(1)乙烯在一定条件下与水反应 ___________________________________,__________
(2)苯与浓硝酸反应______________________________________________,__________
(3)乙酸与丙醇反应______________________________________________,__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠晶体(Na2S2O3·5H2O)又称海波,呈无色透明状,易溶于水,不溶于乙醇,常用作棉织物漂白后的脱氯剂、定量分析中的还原剂。
Ⅰ. Na2S2O3·5H2O的制备
Na2S2O3·5H2O的制备方法有多种,其中亚硫酸钠法是工业和实验室中的主要方法:Na2SO3 + S + 5H2O ![]() Na2S2O3·5H2O
Na2S2O3·5H2O
制备过程如下:
①称取12.6g Na2SO3于100mL烧杯中,加50 mL去离子水搅拌溶解。
②另取4.0 g硫粉于200mL烧杯中,加6 mL乙醇充分搅拌均匀将其润湿,再加入Na2SO3溶液,隔石棉小火加热煮沸,不断搅拌至硫粉几乎全部反应。
③停止加热,待溶液稍冷却后加2 g活性炭,加热煮沸2分钟(脱色)。
④趁热过滤,得滤液至蒸发皿中, ______________、____________________。
⑤过滤、洗涤,用滤纸吸干后,称重,计算产率。
(1)加入的硫粉用乙醇润湿的目的是____________________________。
(2)步骤④趁热过滤的原因_____________________,空格处应采取的操作是_________________、____________________。
(3)步骤⑤洗涤过程中,为防止有部分产品损失,应选用的试剂为___________。
(4)滤液中除Na2S2O3和未反应完全的Na2SO3外,最可能存在的无机杂质是________________,生成该杂质的原因可能是____________________________。
Ⅱ.产品纯度的测定
准确称取1.00 g产品(硫代硫酸钠晶体的摩尔质量为248 g/mol),用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol/L碘标准溶液滴定至终点,消耗21.00 mL。反应的离子方程式为:2S2O32-+I2=S4O62-+2I-。
(5)计算所得产品的纯度为___________(保留三位有效数字),该数据的合理解释可能是__________(不考虑实验操作引起的误差)。
Ⅲ.产品的应用
(6)Na2S2O3常用于脱氯剂,在溶液中易被Cl2氧化为SO42-,该反应的离子方程式为 ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的结构简式为 ![]() ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。
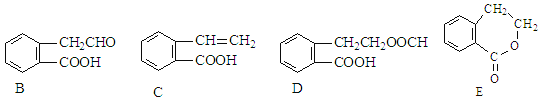
请回答下列问题:
(1)在A~E五种物质中,互为同分异构体的是_______________(填代号)。
(2)写出下列反应的化学方程式和反应类型
A→B:_______________________________________________,反应类型:__________
A→D:_______________________________________________,反应类型:__________
(3)C通过加聚反应能形成高聚物,该高聚物的结构简式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是
A. 食醋除去瓶胆内的水垢:CaCO3+2H+===Ca2++CO2↑+H2O
B. 漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
C. Al溶于NaOH溶液:2Al+2OH-+2H2O===2 AlO+3H2↑
D. 用惰性电极电解硫酸铜溶液:2Cu2++4OH-![]() 2Cu+O2↑+2H2O
2Cu+O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
B |
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性.Cl2>Br2>I2 |
C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
D | 浓HNO3加热 | 有红棕色气体 | HNO3有强氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题越来越受到人们的重视,研究表明氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。
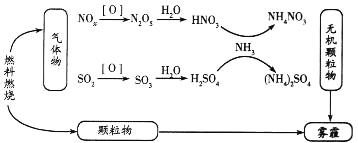
回答下列问题:
(1)NH3的电子式为____________,NH4NO3中含有的化学键是________________:
(2)下列关于雾霾的叙述错误的是________(填序号)
A.雾霾中含有硝酸铵和硫酸铵 B.NH3是形成无机颗粒物的催化剂
C.雾霾的形成与过度施用氮肥有关 D.雾霾的形成过程涉及氧化还原反应
(3)预防含硫化合物雾霾生成的方法之一是将氨气和二氧化硫通入水中,再充入O2充分反应生成一种正盐,该反应的化学方程式为________________________。预防含氮化合物雾霾生成的方法之一是用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸,电解后该溶液的pH_______(填“变大”“变小”或“不变”)。
(4)在有氧条件下,催化剂能催化NH3与NOx反应生成N2,将一定比例的O2、NH3和NOx混合气体匀速通入装有催化剂的反应器中反应,测得反应温度高于380℃时,NOx的去除率迅速下降,其原因之一是催化剂活性下降,另一重要原因是__________________________。在无氧条件下,反应器中NH3能将NO2还原为N2,当生成1mol N2时转移电子________mol(可用分数表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com