
【题目】利用下列实验装置及药品能完成相应实验的是( )
A. 如图用于证明非金属性强弱:Cl>C>S
如图用于证明非金属性强弱:Cl>C>S
B. 如图用于分离I2和NH4Cl
如图用于分离I2和NH4Cl
C. 如图用于测定某NaOH溶液的浓度
如图用于测定某NaOH溶液的浓度
D.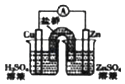 如装置能组成Cu﹣Zn原电池
如装置能组成Cu﹣Zn原电池
科目:高中化学 来源: 题型:
【题目】有五种短周期主族元素,它们在周期表中的位置如图所示,已知R元素的最高正化合价与最低负化合价的代数和为0。
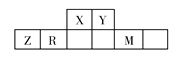
完成下列问题:
(1)Z元素在周期表中的位置是__________________,同周期原子半径最大的元素是____________(填元素符号)。
(2)X的简单氢化物与M的单质,在一定条件下可以发生置换反应,化学方程式为______________,还原产物中含有的化学键类型有____________。
(3)我国发射“神舟”系列飞船的长征火箭,常以X、Y的液态氢化物做燃料。已知X、Y的两种氢化物电子数相等,并且反应时生成两种无毒、无污染的物质。
①写出两种氢化物反应的化学方程式____________________________,反应中氧化剂和还原剂的物质的量之比为____________。
②X的液态氢化物的电子式__________________。
(4)下列说法能证明R、Y非金属性强弱的是____________。
A.R和Y的单质在一定条件下能生成RY2
B.Y单质常温下是气体,R单质是固体
C.Y的氢化物稳定性大于R的氢化物
D.自然界中存在Y单质不存在R单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中可观察到明显现象的是
A. 向盐酸中滴加氢氧化钠溶液
B. 向盐酸中滴加酚酞溶液
C. 向氯化镁溶液中滴加氢氧化钡溶液
D. 将铜丝放入到硫酸铝溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)2NH3(g)△H.
(1)已知每破坏1mol有关化学键需要的能量如表:
H﹣H | N﹣H | N﹣N | N |
435.9KJ | 390.8KJ | 192.8KJ | 945.8KJ |
则△H= .
(2)在恒温、恒压容器中,氨体积比1:3加入N2和H2进行合成氨反应,达到平衡后,再向容器中充入适量氨气,达到新平衡时,c(H2)将(填“增大”“减小”或“不变”)
(3)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示. 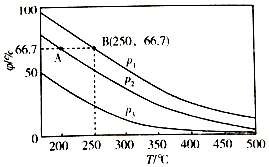
①其中,p1、p2和p3由大到小的顺序是 , 其原因是 .
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)vB(N2)(填“>”“<”或“=”)
③若在250℃、p1条件下,反应达到平衡时容器的体积为1L,则该条件下合成氨的平衡常数K=(保留一位小数).
(4)H2NCOONH4是工业由氨气合成尿素的中间产物.在一定温度下、体积不变的密闭容器中发生反应:H2NCOONH4(s)2NH3(g)+CO2(g),能说明该反应达到平衡状态的是(填序号). ①混合气体的压强不变
②混合气体的密度不变
③混合气体的总物质的量不变
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①漏斗、②试管、③分液漏斗、④容量瓶、⑤蒸馏烧瓶,常用于物质分离的是 ( )
A. ①③⑤ B. ②③⑤ C. ②④⑤ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色溶液中能大量共存的离子组是
A. HCO3-、Na+、OH-、K+ B. CH3COO-、Ba2+、MnO4-、H+
C. NO3-、H+、Cl-、Cu2+ D. SO42-、K+、Cl-、NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
Ⅰ.探究同周期元素性质的递变规律
(1)相同条件下,将钠、镁、铝各1 mol分别投入到足量的同浓度的稀盐酸中,试预测实验结果:_______与稀盐酸反应最剧烈;______与稀盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_____________________________。
Ⅱ.探究同主族元素非金属性的递变规律
某研究性学习小组设计了一组实验来探究ⅦA族元素原子的得电子能力强弱规律。下图中A、B、C是三个可供选择制取氯气的装置,装置D的玻璃管中①、②处依次放置蘸有NaBr溶液、NaOH浓溶液的棉球。
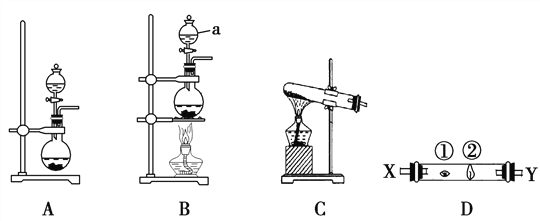
(3)写出装置B中仪器a的名称 ________________。
(4)实验室制取氯气还可采用如下原理:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,依据该反应原理选择_____________(填“A”或“B”或“C”)装置制取氯气。
(5)反应装置的导气管连接装置D的X导管,试回答下列问题:
①处发生反应的离子方程式为________________________________;
②处发生反应的离子方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在密闭容器中反应A(g)+3B(g)2C(g) 在一定温度下达到平衡,
(1)在平衡时测得各物质的物质的量分别为n(A)=1.0mol、n(B)=0.4mol、n(C)=0.4mol,此时容器体积为2L,则此条件下的平衡常数K= .
(2)若保持温度和压强不变,在(1)中平衡中向上述容器中通入0.36mol A (g),平衡将(填“正向”、“逆向”或“不”)移动,用简要的计算过程说明理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素X、Y、Z、W的相对位置如表,元素X的原子核外电子数是Z的2倍。下列说法不正确的是
![]()
A. W元素的简单气态氢化物的热稳定性比Z元素的简单气态氢化物的高
B. 气体分子(ZW)2的结构式为N≡C—C≡N
C. X、Y、W三种元素的简单离子半径最大的是Y
D. 元素X可在元素W单质中燃烧。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com