
| A. | (3m+n)mol | B. | ($\frac{5m}{2}$+$\frac{n}{2}$-3p)mol | C. | ($\frac{5m}{2}$+$\frac{n}{2}$)mol | D. | (3m+n+2p)mol |
分析 无论乙炔和氢气反应程度如何,根据原子守恒,混合物中各元素的原子个数不变,物质的量不变.先计算出碳原子、氢原子的物质的量,然后根据碳氢原子的物质的量求出所需氧气的物质的量.
解答 解:无论乙炔和氢气反应程度如何,根据原子守恒,混合物中各元素的原子个数不变,物质的量不变,则碳氢元素的物质的量分别为:
C2H2~2C~2H
1 2 2
mmol 2mmol 2mmol
H2~2H
1 2
nmol 2nmol
所以混合物中碳原子的物质的量为2mmol,氢原子的物质的量为(2m+2n)mol,
根据碳氢元素完全燃烧可知C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O,
所以混合气体完全燃烧所需氧气为2mmol+$\frac{2m+2n}{4}$mol=$\frac{5m+n}{2}$mol=($\frac{5m}{2}$+$\frac{n}{2}$)mol,
故选C.
点评 本题考查了化合物反应的计算,题目难度不大,注意掌握质量守恒定律在化学计算中的应用,试题培养了学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L的盐酸15mL | B. | 0.15 mol/L 的硫酸溶液8mL | ||
| C. | 0.2 mol/L 的盐酸12mL | D. | 18 mol/L的浓硫酸15mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用福尔马林保存生物标本 | |
| B. | 试管上沾有苯酚时,用水洗 | |
| C. | 实验室不慎将Hg洒在地上时,立即用硫粉覆盖 | |
| D. | 皮肤上沾有苯酚时,立即用酒精擦洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
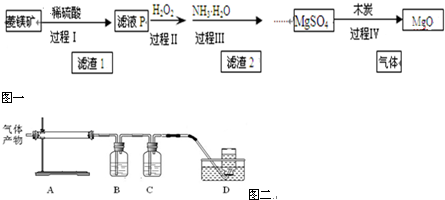
| Mg(OH)2 | Fe(OH)3 | Fe(OH)2 | |
| 开始沉淀的pH | 10.4 | 1.9 | 7.0 |
| 沉淀完全的pH | 12.4 | 3.2 | 9.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 Z>Y>X | |
| B. | Z的非金属性最强 | |
| C. | 氢化物还原性XH3>H2Y>HZ,稳定性XH3>H2Y>HZ | |
| D. | 最高氧化物对应水化物H3XO4酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com