
1体积某烃的蒸气完全燃烧生成的CO2比水蒸气少1体积(在同温同压下测定),0.1 mol该烃完全燃烧的产物全部被碱石灰吸收,碱石灰增重51.4 g。试解答:
(1)求该烃的分子式;
(2)若该烃的一氯代物只有一种,试写出该烃的结构简式并用系统命名法命名。
(1)C8H18 (2)(CH3)3CC(CH3)3;2,2,3,3四甲基丁烷
解析 由于在相同条件下1体积某烃的蒸气完全燃烧生成的CO2比水蒸气少1体积,则该烃的分子式为CnH2n+2,0.1 mol该烃完全燃烧生成的CO2与H2O的物质的量的关系如下:①n(CO2)=n(H2O)-0.1 mol,又因为碱石灰增重51.4 g,即CO2和H2O的质量之和为51.4克。
所以有:②44×n(CO2)+18×n(H2O)=51.4 g
将①②联立,解方程组得:n(CO2)=0.8 mol,n(H2O)=0.9 mol。
所以0.1 mol烃中有0.8 mol碳原子和1.8 mol氢原子,所以分子式是C8H18。
由于该烃的一氯代物只有一种,则该烃分子中只有一类氢原子,根据分子结构的对称性进行分析,可知该烃的结构式如下: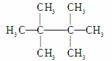 ,其名称为2,2,3,3四甲基丁烷。
,其名称为2,2,3,3四甲基丁烷。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
为进行Ⅰ项实验,从Ⅱ项中选出一种试剂,从Ⅲ项中选出一种合适的操作方法:
| Ⅰ实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| (1)除去苯中的苯酚 | A.CaO | a.分液 | (1) | ||
| (2)除去工业酒精中的水 | B.Na2CO3溶液 | b.蒸馏 | (2) | ||
| (3)除去乙酸乙酯中的乙酸 | C.NaCl | c.过滤 | (3) | ||
| (4)除去肥皂中的甘油 | D.NaOH | d.盐析 | (4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X和元素Y,元素X原子的最外层电子数为a,次外层电子数为b;元素Y原子的M层电子数为(a-b),L层电子数为(a+b),则下列说法正确的是 ( )。
A.可形成YX型化合物
B.Y原子质子数比X原子大6
C.X、Y的单质在化学反应中均易得到电子
D.X、Y的单质均易与氯气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”(Funiulele)。有一种有机物的键线式也酷似牛,故称为牛式二烯炔醇(cowenynenynol)。下列有关说法不正确的是( )
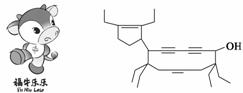
A.牛式二烯炔醇分子内含有两种官能团
B.牛式二烯炔醇能够发生加聚反应得到高分子化合物
C.牛式二烯炔醇在一定条件下能与乙酸发生酯化反应
D.牛式二烯炔醇可使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出下列化合物的名称或结构简式:

(2)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱,经我国科学家研究发现其结构如下:
①麻黄素中含氧官能团的名称是________,属于________类(填“醇”或“酚”)。
②下列各物质:
 与麻黄素互为同分异构体的是________(填字母,下同),互为同系物的是________。
与麻黄素互为同分异构体的是________(填字母,下同),互为同系物的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种有机物①(CH3)2CHCH(CH3)2,②(CH3)2C(CH3)2,③CH3(CH2)2CH(CH3)2,④CH3CH2C(CH3)3有关这四种物质的下列叙述不正确的是( )
A.①和②互为同分异构体,①和④互为同系物 B.④的一氯代物有三种
C.②不可能由烯烃与氢气加成而获得 D.能通过加氢反应得到③的炔烃有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
江水受到污染,其污染的主要原因是 ( )。
①工业生产中废液的任意排放 ②雨水和土壤的长期接触 ③农业生产中农药、化肥的过量施用 ④城市生活污水的任意排放
A.①②③ B.②③④
C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示:
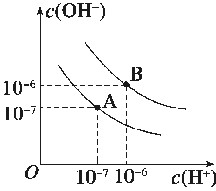
(1)若以A点表示25℃时水电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从______增加到________。
(2)将pH=8的氢氧化钡溶液与pH=5的盐酸溶液混合并保持100℃恒温,欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为________。
(3)已知AnBm的离子积K=[c(Am+)]n·[c(Bn-)]m,式中c(Am+)和c(Bn-)表示离子的物质的量浓度。在某温度下,氢氧化钙溶解度为0.74 g,其饱和溶液密度设为1 g/cm3,其离子积为K=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com