
| A. | 运用蒸馏的方法,可以分离沸点相差较大的固体混合物 | |
| B. | 铁的化合物应用十分广泛,如FeCl3、FeSO4是优良的净水剂 | |
| C. | 镁燃烧发出耀眼的白光,常用于制造信号弹和焰火 | |
| D. | 工业上以氯气和石灰乳为原料制造漂白粉,漂白粉主要成分为Ca(ClO)2和CaCl2 |
分析 A.分离沸点相差较大的互溶液体混合物,选择蒸馏;
B.FeCl3、FeSO4均可水解生成胶体;
C.Mg燃烧生成MgO,发出耀眼的白光;
D.氯气与石灰乳反应生成氯化钙、次氯酸钙和水.
解答 解:A.分离沸点相差较大的互溶液体混合物,选择蒸馏,蒸馏不能分离固体混合物,故A错误;
B.FeCl3、FeSO4均可水解生成胶体,则可作优良的净水剂,故B正确;
C.Mg燃烧生成MgO,发出耀眼的白光,则常用于制造信号弹和焰火,故C正确;
D.氯气与石灰乳反应生成氯化钙、次氯酸钙和水,则漂白粉主要成分为Ca(ClO)2和CaCl2,故D正确;
故选A.
点评 本题考查较综合,为高频考点,把握物质的性质、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 230 | a |
| A. | 369 | B. | 384 | C. | 469 | D. | 499 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Al3+、HCO3-、NO3- | B. | Fe3+、SCN-、Cl-、K+ | ||
| C. | NH4+、Na+、CH3COO-、NO3- | D. | Na+、NO3-、ClO-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| T |
| A. | X、Z、W元素的原子半径依次递增 | |
| B. | T元素的非金属性比Z弱 | |
| C. | YX2晶体熔化、液态WX3气化均需克服分子间作用力 | |
| D. | Y、Z、W元素在自然界中均不能以游离态存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
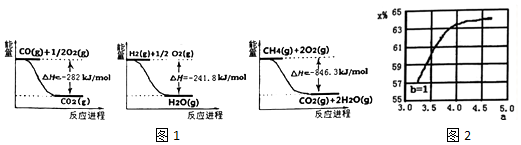
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 加入的物质 | 结论 | |
| A | 0.05molCH3COONa | $\frac{c(C{H}_{3}CO{O}^{-})}{c(N{a}^{+})}$增大 |
| B | 0.05molNaHSO4 | c(CH3COO-)+c(CH3COOH)=c(Na+)-c(SO42-) |
| C | 0.05molNH4Cl | 溶液中性,水的电离程度减小 |
| D | 50mLH2O | 由水电离出的c(H+)•c(OH-)减小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,NA个水分子所占的体积约为22.4L | |
| B. | 5.6g铁与氯气完全反应,失去电子的数目为0.2NA | |
| C. | 1mol氯气发生化学反应,转移的电子数必为2NA | |
| D. | CH4的摩尔质量与NA个CH4分子的质量在数值上相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com