(2013?淄博一模)请运用化学反应原理的相关知识研究元素及其化合物的性质.
(1)工业上一般以CO和H
2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+2H
2(g)?CH
3OH(g)△H
1=-116KJ?mol
-1又知:CO(g)+
O
2(g)═CO
2(g)△H
2=-283KJ?mol
-1 H
2(g)+
O
2(g)═H
2O(g)△H
3=-242KJ?mol
-1 H
2(g)+
O
2(g)═H
2O(g)△H
4=-286KJ?mol
-1则甲醇的燃烧热为
-739kJ?mol-1
-739kJ?mol-1
.
(2)T℃时,向2L密闭容器中充入4mol CO和6mol H
2,5min后达平衡时CH
3OH物质的量为2mol.该反应的速率v(H
2)为
0.4mol/(L?min)
0.4mol/(L?min)
;下列措施中有利于增大该反应的反应速率且提高转化率的是
d
d
.
a.随时将CH
3OH与反应混合物分离
b.降低反应温度
c.使用高效催化剂
d.增大体系压强
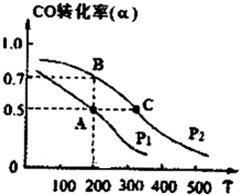
(3)在密闭容器中充有10mol CO与20mol H
2,在催化剂作用下反应生成甲醇,CO的转化率(a)与温度(T)、压强(P)的关系如图所示.
①A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间,t
A大于
大于
t
c(填“大于”、“小于’’或“等于“).
②若A点时容器的体积为10L,该温度下B点的平衡常数K=
1
1
.
(4)Na
2SO
3的水溶液呈
碱
碱
(填“酸”、“中”、‘‘碱”)性,原因是(用离子方程式表示):
SO32-+H2O?HSO3-+OH-
SO32-+H2O?HSO3-+OH-
;把CaCO
3浊液滴入l.0mol/L的Na
2SO
3溶液中,能否产生CaSO
3沉淀?若不能,说明原因;若可行,请简述判断依据及转化过程
可行,判断依据是:由Ksp(CaSO3)/Ksp(CaCO3)=50知,当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变;转化过程为:把CaCO3浊液滴入0.1mol/L的Na2SO3溶液中时,溶液中的c(Ca2+)与c(SO32-)之积大于Ksp(CaSO3),生成CaSO3沉淀,导致溶液中c(Ca2+)减小,使CaCO3的沉淀溶解平衡CaCO3?Ca2++CO32-,向着溶解的方向移动,导致CaCO3溶解.
可行,判断依据是:由Ksp(CaSO3)/Ksp(CaCO3)=50知,当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变;转化过程为:把CaCO3浊液滴入0.1mol/L的Na2SO3溶液中时,溶液中的c(Ca2+)与c(SO32-)之积大于Ksp(CaSO3),生成CaSO3沉淀,导致溶液中c(Ca2+)减小,使CaCO3的沉淀溶解平衡CaCO3?Ca2++CO32-,向着溶解的方向移动,导致CaCO3溶解.
(已知:Ksp(CaSO
3)=1.4×10
-7,Ksp(CaCO
3)=2.8×10
-9).

 (2013?泰安三模)SO2、NO、NO2、CO都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.
(2013?泰安三模)SO2、NO、NO2、CO都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题. CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
 (2013?淄博一模)请运用化学反应原理的相关知识研究元素及其化合物的性质.
(2013?淄博一模)请运用化学反应原理的相关知识研究元素及其化合物的性质.
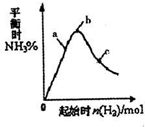 工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.
工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.