
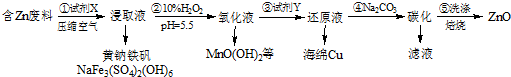
分析 铁、铜、锰能与盐酸反应生成Fe2+、Zn2+、Mn2+;Mn2+可与双氧水反应生成MnO(OH)2↓;锌能与铜离子反应生成铜单质;硫酸锌能与碳酸钠反应生成硫酸钠和碳酸锌,碳酸锌受热分解生成氧化锌和水,
(1)铁、铜、锰能与盐酸反应生成Fe2+、Zn2+、Mn2+;
(2)Mn2+可与双氧水反应生成MnO(OH)2↓;锌能与铜离子反应生成铜单质;硫酸锌能与碳酸钠反应生成硫酸钠和碳酸锌;
(3)滴加BaCl2溶液,若无白色沉淀生成,则表明已洗涤干净;
(4)碱式碳酸锌6.82 g,充分灼烧后测得残留物质为氧化锌,质量为4.86 g,锌的质量为3.9g.将所得气体是二氧化碳,沉淀碳酸钙是2.0 g,物质的量为0.02mol.碳酸根的物质的量为0.02mol.根据电荷守恒得氢氧根的物质的量为X=0.08mol.由碱式碳酸锌6.82 g减去锌的质量,碳酸根和氢氧根的质量,剩下的就为水的质量.
解答 解:铁、铜、锰能与盐酸反应生成Fe2+、Zn2+、Mn2+;Mn2+可与双氧水反应生成MnO(OH)2↓;锌能与铜离子反应生成铜单质;硫酸锌能与碳酸钠反应生成硫酸钠和碳酸锌,碳酸锌受热分解生成氧化锌和水,
(1)铁、铜、锰能与盐酸反应生成Fe2+、Zn2+、Mn2+,Fe2+能被氧化为Fe3+,浸取液课得到黄钠铁钒,说明X为Na2SO4和H2SO4的混合液,
故答案为:Fe3+;Cu2+;H2SO4;
(2)Mn2+可与双氧水反应生成MnO(OH)2↓,离子方程式:Mn2++H2O2+H2O═MnO(OH)2↓+2H+;锌能与铜离子反应生成铜单质;硫酸锌能与碳酸钠反应生成硫酸钠和碳酸锌,Na2SO4可以循环使用,
故答案为:Mn2++H2O2+H2O═MnO(OH)2↓+2H+;Zn;Na2SO4;
(3)检验沉淀是否洗涤干净的操作方法为:取最后一次洗涤滤液滴加BaCl2溶液,若无白色沉淀生成,则表明已洗涤干净,
故答案为:取最后一次洗涤滤液1~2mL于试管中,向其中滴加BaCl2溶液,若无白色沉淀生成,则表明已洗涤干净;
(4)碱式碳酸锌6.82 g,充分灼烧后测得残留物质为氧化锌,质量为4.86 g,物质的量为:$\frac{4.86g}{81g/mol}$=0.06mol,锌的质量为3.9g.将所得气体是二氧化碳,沉淀碳酸钙是2.0 g,物质的量为0.02mol.碳酸根的物质的量为0.02mol.
根据电荷守恒:0.06mol×2=0.02mol×2+X,
得氢氧根的物质的量为X=0.08mol,
由碱式碳酸锌6.82 g减去锌的质量,碳酸根和氢氧根的质量,剩下的就为水的质量:6.82-3.9-0.02×60-0.08×17=0.36g,物质的量为0.02mol,
故碱式碳酸锌的组成ZnCO3•2Zn(OH)2•H2O 或Zn3(OH)4CO3•H2O,
故答案为:ZnCO3•2Zn(OH)2•H2O或Zn3(OH)4CO3•H2O.
点评 本题考查物质的分离与提纯方法的综合应用及制备实验方案的设计,题目难度中等,涉及化学计算、氧化还原反应和离子反应方程式的书写、化学式的判断等知识,明确实验目的、实验原理为解答关键,试题培养了学生的分析、理解能力及化学实验能力.


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:选择题
| A. | CaO2具有氧化性,对面粉可能具有增白作用 | |
| B. | CaO2与水反应时,每产生1molO2转移电子4mol | |
| C. | CaO2中阴阳离子的个数比为1:1 | |
| D. | CaO2与CO2反应的化学方程式为2CaO2+2CO2═2CaCO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界中不存在游离态的硫,且S可溶于CS2 | |
| B. | SO2和SO3都是酸性氧化物,二者的水溶液都是强酸 | |
| C. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 | |
| D. | 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl- NO3- Ba2+ Fe3+ | B. | SO42- S2- Al3+ Mg2+ | ||
| C. | Na+ K+ SO42- Cl- | D. | NH4+ Ba2+ Cl- HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 碳酸氢钠溶液中滴加氢氧化钠溶液:HCO3-+OH-═CO2+H2O | |
| D. | 过氧化钠与水的反应:2Na2O2+2H2O═4Na++4OH-+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
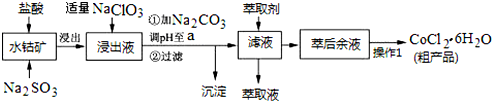
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
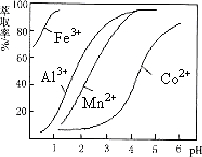
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数和中子数均为6的碳原子:${\;}_{6}^{6}C$ | |
| B. | 硫离子的结构示意图: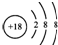 | |
| C. | 氢氧化钠的电子式: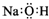 | |
| D. | 2-丙醇的结构简式: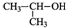 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅酸盐是良好的半导体材料 | B. | 硅是地壳中含量最多的元素 | ||
| C. | SiO2不溶于水,也不溶于任何酸 | D. | 二氧化硅用于制作光导纤维 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com