
(17分)降低太气中CO2含量及有效开发利用CO2,是科学家研究的重要课题。
(1)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)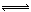 CH3OCH3(g)+3H2O(g) △H=-122.4kJ·mol-1
CH3OCH3(g)+3H2O(g) △H=-122.4kJ·mol-1
①某温度下,将2.0molCO2(g)和6.0molH2(g)充入体积可变的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化如下表所示。
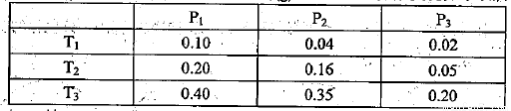
则Pl P3(填“>”“<”或“=”,下同)。若T1、Pl,T3、P3时平衡常数分别为K1、K3,
则K1 K3。T1、Pl时H2的平衡转化率为 。
②一定条件下,t上述反应在密闭容器中达平衡。当仅改变影响反应的一个条件,引起的下列变化能说明平衡一定向正反应方向移动的是____ 。
A.反应物的浓度降低 B.容器内压强增大
C.正反应速率大于逆反应速率 D.化学平衡常数K增大
(2)碳酸氢钾溶液加水稀释,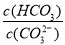 (填“增大”“不变”或“减小”)。用碳酸钾溶液吸收空气中CO2,当溶渡呈中性时,下列关系或说法正确的是 。
(填“增大”“不变”或“减小”)。用碳酸钾溶液吸收空气中CO2,当溶渡呈中性时,下列关系或说法正确的是 。
A.c(K+)=2c(CO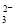 )+c(HCO
)+c(HCO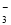 )+c(H2CO3)
)+c(H2CO3)
b.c(HCO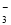 )
)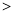 c(CO
c(CO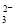 )
)
c.降低温度,c(H+)·c(OH-)不变
(3)向盛有FeCl3溶液的试管中滴加少量碳酸钾溶液,立即产生气体,溶液颜色加深,用激光笔照射能产生丁达尔效应,反应的离子方程式为 。
(17分)
(1)① > (2分) < (2分)57.14%(2分)② c d(2分)
(2)减小(3分) b(3分)
(3)2Fe3++3CO32?+3H2O=2Fe(OH)3(胶体)+3CO2↑(3分)
【解析】
试题分析:(1)①相同温度下,P1时CH3OCH3物质的量分数大于P3时CH3OCH3物质的量分数,根据化学方程式,加压平衡向右移动,所以P1 > P3;T3时CH3OCH3物质的量分数大于T1时CH3OCH3物质的量分数,因为该反应为放热反应,升高温度,平衡向逆反应方向移动,所以K1<K3;根据“三段式”进行计算,设生成的CH3OCH3的物质的量为x,则
2CO2(g)+6H2(g)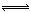 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
起始物质的量(mol) 2 6 0 0
转化物质的量(mol) 2x 6x x 3x
平衡物质的量(mol) 2— 2x 6—6x x 3x
则x/(8-4x)=0.1,解得x=0.5714,H2的平衡转化率=6x/6×100% =57.14%
②a、生成物的浓度也可能降低,如增大体积,平衡向逆反应方向移动,错误;b、如果加入惰性气体使容器内压强增大,平衡不移动,错误;c、正反应速率大于逆反应速率,平衡一定向正反应方向移动,正确;d、化学平衡常数K增大,说明平衡一定向正反应方向移动,正确。
(2)碳酸氢钾溶液加水稀释,HCO3?的电离平衡向右移动,所以c(HCO3?)/c(CO32?)减小;因为K2CO3和KHCO3溶液呈碱性,所以当溶渡呈中性时,CO2过量,溶液的溶质为KHCO3和H2CO3,故b项正确,根据电荷守恒可得c(K+)=2c(CO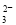 )+c(HCO
)+c(HCO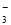 ),故a项错误,降低温度,水的电离平衡向左移动,c(H+)·c(OH-)减小,c项错误。
),故a项错误,降低温度,水的电离平衡向左移动,c(H+)·c(OH-)减小,c项错误。
(3)产生气体,溶液颜色加深,用激光笔照射能产生丁达尔效应,说明生成了CO2气体和Fe(OH)3胶体,所以离子方程式为:2Fe3++3CO32?+3H2O=2Fe(OH)3(胶体)+3CO2↑。
考点:本题考查化学平衡移动、电离平衡、离子浓度比较、离子方程式的书写、化学计算。


科目:高中化学 来源:2013-2014山东省潍坊市高三4月模拟考试理综化学试卷(解析版) 题型:计算题
(17分)随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题。
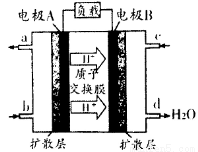
(1)汽车尾气的大量排放是造成空气污染的重要因素之一,发展燃料电池汽车可以有效地解决上述问题。直接甲醇燃料电池(DMFC)不会产生有害产物,能量转换效率比内燃机要高2~3倍,电池结构如图所示,c处通入的物质为为______,外电路中电子从______到______(填“A”或“B”)移动,写出电池负极的电极反应方程式
(2)工业废水中常含有一定量的Cr2O72-,会对人类及生态系统产生很大损害,电解法是处理铬污染的常用方法。该法用Fe做电极电解含Cr2O72-的酸性废水,电解时,在阴极上有大量气泡生成,并产生Cr(OH)3、Fe(0H)3沉淀。
①反应中,1molCr2O72-完全生成Cr(OH)3沉淀,外电路通过电子的物质的量为_________ mol。
②常温下,Cr(OH)3的溶度积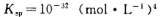 ,当Cr3+浓度小于10
,当Cr3+浓度小于10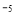 mol
mol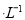 时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。
时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。
(3)含氨废水易引发水体富营养化。向NH4Cl溶液中加入少量NaOH固体,溶液中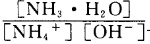 ________(填“增大”“减小”或“不变”);25
________(填“增大”“减小”或“不变”);25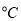 时,NH3?H2O的电离平衡常数
时,NH3?H2O的电离平衡常数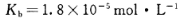 ,该温度下,1mol
,该温度下,1mol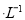 的NH4Cl溶液中
的NH4Cl溶液中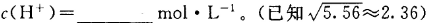
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列物质中,化学键类型完全相同的是
A.CaBr2与HCl B.MgCl2与Na2S
C.KOH与NaCl D.H2O与NaCl
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
(17分)H2O2是一种强氧化剂,被广泛应用于水处理及卫生消毒等方面。
(1)H2O2不稳定,当其中含Fe2+时,会发生反应:
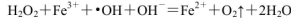 ,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。
,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。
(2)下表是在常压、60℃和不同pH条件下,6mL30% H2O2在60min内释放出氧气的体积。则下列说法正确的是___________。
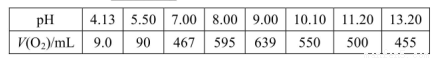
a.pH越大,H2O2的分解速率越大
b.pH在9左右,H2O2的分解速率最大
c.6mL 30% H2O2分解最多释放出的氧气的体积为639mL
d. pH=5.50时,0~60min内,v(O2)=1.5mL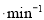
(3)溶液中H2O2的残留量可用一定浓度的酸性KMnO4溶液来测定,反应中MnO4-
被还原为Mn2+,该反应的离子方程式为______________。
(4)科学工作者以Ir-Ru/Ti为阳极、ACFC为阴极,在酸性环境、不断通入空气的条件下直接电解水来制备H2O2。电解过程中,阳极区溶液的pH_ (填“增大”“不变”或“减小”),阴极产生H2O2的电极反应式为_______。若不通空气,则阴极得到的产物是_______ 。
(5)己知断裂1mol化学键所需的能量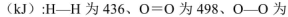
143,H-O为463。则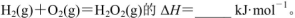 .
.
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
化学与生产和生活密切相关,下列说法正确的是
A.误食重金属盐引起人体中毒,可喝大量的食盐水解毒
B.变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
C.浸泡过高锰酸钾溶液的硅藻土放于水果箱内是为了延长水果保鲜期
D.安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三二模理综化学试卷(解析版) 题型:选择题
丙烯醇在一定条件下可转化为丙烯醛: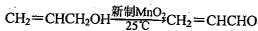 。下列有关说法错误的是
。下列有关说法错误的是
A.丙烯醇与丙醛(CH3CH2CHO)互为同分异构体
B.丙烯醇含有两种官能团
C.可用新制Cu(OH)2鉴别丙烯醛和丙烯醇
D.此转化过程中丙烯醇被还原
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高一下学期期末考试化学试卷(解析版) 题型:填空题
(15分)某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
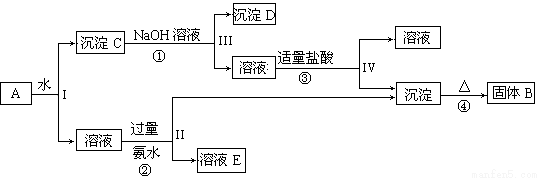
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B ;C ;
沉淀D ;溶液E 。
(3)写出①、②、③、④四个反应方程式(是离子反应的写出离子方程式)
① ;② ;
③ ; ④ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市高一5月质量检测化学试卷(解析版) 题型:选择题
反应H2(g)+ I2(g) 
 2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )
2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )
①单位时间内断裂n mol H-H键的同时形成2n mol H-I键 ②单位时间内生成n molI2的同时生成2n molHI
A.②④⑤⑥ B.②③④⑤ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高一化学试卷(解析版) 题型:填空题
(8分)
某些化学反应可用下式表示A+B→→C+D+H2O。请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式: 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 。
(3)若A、C均含有铝元素。①当B是盐酸时,C是 ;
②当B是NaOH时,C是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com