
| ʱ��/min | ��0 | 30 | 70 | 80 | 100 |
| n��CO2��/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
���� ��1������֪�Ȼ�ѧ����ʽ��������ȼ���ȵ��Ȼ�ѧ����ʽ���ۺ����ø�˹������⣻
��2���μӰ�ˮ�Ĺ����У���ˮ���������OH-��ˮ�ĵ���ƽ�����������ã���֪���ݵ���غ㣬����Һ��笠����ӵ����ʵ�����
��3���ٻ�ѧƽ�⽨���Ǵӷ�Ӧ��Ͷ�Ͻ���ƽ��״̬�ģ����Դӿ�ʼ��ƽ�ⷴӦ���Ũ���ڲ��ϼ��٣�Ũ��ԽС����ԽС��ƽ�ⳣ������������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ���ݴη��˻���
����100minʱ�����������������䣬���������г���0.050mol CO2��0.20mol NH3�൱��ԭƽ��ϵ��ѹ��
�ۼ���ƽ��Ũ�ȣ�ƽ��ʱ��c��CO2��=0.04��2=0.02mol/L��c��NH3��=��0.4-0.06��2����2=0.14mol/L��c��H2O��=0.06��2=0.03mol/L��ƽ�ⳣ������������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ���ݴη��˻���
�������¶ȣ�ƽ�������ƶ���������ת���ʼ�С��
�ݵ�һ�������ǵ缫��Ӧʽ����д�����ȴӼ�̬�仯�ϣ��ж������ϲ���������Ȼ����ݻ��ϼ۵ı仯�͵��ӵ�ʧ�غ㣬����غ㣬��д���缫��Ӧʽ��
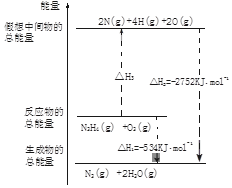
��� �⣺��1��NH3��g���ڴ�����ȼ���������������������������Ȼ�ѧ����ʽ��ʵ�����ǿ����˹���ɵ�Ӧ�ã�����H2��g����ȼ����Ϊ285.8kJ•mol-1����H2��g��+1/2O2��g��=H2O��l����H=-285.8kJ•mol-1���٣��ٽ����֪�ģ�N2��g��+3H2��g��?2NH3��g����H=-92.4 kJ•mol-1����
���١�3-�ڣ���2���ɵõ���4NH3��g��+3O2��g��=2N2��g��+6H2O��l����H=-1530 kJ•mol -1��
�ʴ�Ϊ��4NH3��g��+3O2��g��=2N2��g��+6H2O��l����H=-1530 kJ•mol -1��
��2������NH4��2SO4��Һ�еμ�ϡ��ˮ�Ĺ�����ˮ�ĵ���ƽ���ܵ����ƣ�H2O?H++OH-��������ͼ�ƽ�������ƶ�����˼Ӱ�ˮ��ˮ�ĵ����������ƶ�����amol��NH4��2SO4����ˮ�������Һ�еμ�VLϡ��ˮ����Һ�����Կ�֪��c��OH-��=10-7mol/L����ƽ��ʱNH3•H2O�����ʵ���Ϊx����Һ�����Ϊb��
��NH3•H2O?NH4++OH-
$\frac{x}{b}$ $\frac{2a}{b}$ 10-7
�ɵ���ƽ�ⳣ����֪��$\frac{\frac{2a}{b}��1{0}^{-7}}{\frac{x}{b}}$=2��10-5��֮�ã�x=$\frac{a}{100}$����c��NH3•H2O��=$\frac{a}{100V}$��
�ʴ�Ϊ������$\frac{a}{100V}$��
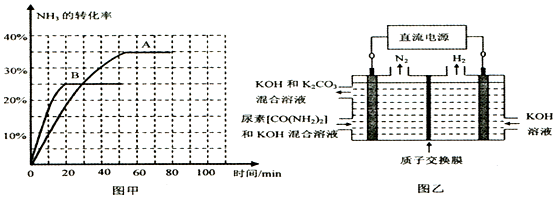
��3���ٴӱ��е����ݿ�֪��80minʱ�Ѿ��ﵽƽ�⣬v����H2O��=v����H2O��=v����CO2������20minʱδ�ﵽƽ�⣬v����CO2������80minʱv����CO2������ˣ�20minʱv����CO2������80minʱv����H2O������t��ʱ��CO2��g��+2NH3��g��?CO��NH2��2��l��+H2O��g����H��0���÷�Ӧ��ƽ�ⳣ������ʽΪK=$\frac{c��{H}_{2}O��}{c��C{O}_{2}��{c}^{2}��N{H}_{3}��}$��
�ʴ�Ϊ������$\frac{c��{H}_{2}O��}{c��C{O}_{2}��{c}^{2}��N{H}_{3}��}$��
�ڵ�һ��Ͷ����0.10molCO2��0.40molNH3���ڶ���Ͷ����0.15molCO2��0.60molNH3���ڶ���Ͷ�Ͻ�����ƽ��״̬�൱���ٵ�һ��Ͷ�Ͻ���ƽ��Ļ������ټ�ѹ��ƽ�������ƶ������CO2��ת���ʽ����ʴ�Ϊ������
��ƽ��ʱ��c��CO2��=0.04��2=0.02mol/L��c��NH3��=��0.4-0.06��2����2=0.14mol/L��c��H2O��=0.06��2=0.03mol/L����K=$\frac{c��{H}_{2}O��}{c��C{O}_{2}��{c}^{2}��N{H}_{3}��}$=$\frac{0.03}{0.02��0.1{4}^{2}}$=76.53���ʴ�Ϊ��76.53��
����������ʽ�����30minʱNH3��ת����Ϊ20%��70minʱNH3��ת����Ϊ30%��Ȼ��ģ�����������Ƴ����ߣ�ע��70minǰ��ͼ���ܻ���ֱ�ߣ����������Ȼ��Ƿ��ȷ�Ӧ���¶�����ʱ���ﵽƽ���ʱ�䶼�����̣��÷�Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ�ƽ��������ƶ�������NH3��ת���ʻ��С���ʴ�Ϊ��B��
�ݵ缫��ӦʽΪ��CO��NH2��2-6e-+8OH-=CO32-+N2��+6H2O���ܷ�Ӧ��CO��NH2��2+2OH-=CO32-+N2��+3H2��
�� 1molCO��NH2��2 ��4mol���壬
60g 89.6L
15g 22.4L��
�ʴ�Ϊ��CO��NH2��2-6e-+8OH-=CO32-+N2��+6H2O��15��
���� ���⿼�鰱����ʵ�����Ʒ���ԭ������˹���ɵ�Ӧ�á���ѧƽ����ƶ�������ƽ�ⳣ������Чƽ��͵绯ѧ�����֪ʶ���漰��֪ʶ��࣬��Ŀ�Ѷ��еȣ�


 �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����£�N2H4���ǵ������ֳ���������ڿ�ѧ����������������Ҫ��Ӧ�ã�
�����£�N2H4���ǵ������ֳ���������ڿ�ѧ����������������Ҫ��Ӧ�ã� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
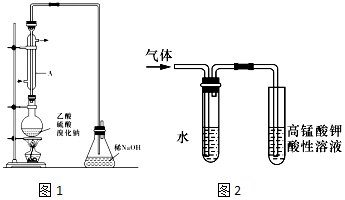
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ˮ����������ľ�ķ����������Ҫ�ɷ��ǣ�д��ѧʽ��Na2SiO3��д����ҵ�����ֹ�Ļ�ѧ����ʽSiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO�������������£��������衢̼�ۡ����������ʵ���֮��3��6��2��Ӧ�������ɵ������մɣ�һ���������ǽ������ϣ��������¡���ĥ�������������ԣ�����һ�����廯����÷�Ӧ�Ļ�ѧ����ʽΪ3SiO2+2N2+6C $\frac{\underline{\;����\;}}{\;}$Si3N4+6CO��
��ˮ����������ľ�ķ����������Ҫ�ɷ��ǣ�д��ѧʽ��Na2SiO3��д����ҵ�����ֹ�Ļ�ѧ����ʽSiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO�������������£��������衢̼�ۡ����������ʵ���֮��3��6��2��Ӧ�������ɵ������մɣ�һ���������ǽ������ϣ��������¡���ĥ�������������ԣ�����һ�����廯����÷�Ӧ�Ļ�ѧ����ʽΪ3SiO2+2N2+6C $\frac{\underline{\;����\;}}{\;}$Si3N4+6CO���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ɫ��Һ�м����Ȼ�����Һ�а�ɫ�������ɣ��ټ����ᣬ��������ʧ������Һ��һ������SO42- | |
| B�� | �ò�˿պȡ����ij��Һ������ɫ��Ӧ������ʻ�ɫ������Һһ����������Һ | |
| C�� | �μ����ữ��AgNO3��Һ�������ɫ������˵������Һһ������Cl- | |
| D�� | ��ij��Һ�еμ�KSCN��Һ����Һ����ɫ���μ���ˮ����Һ�Ժ�ɫ������Һ��һ����Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�ۡ���ˮ�ͱ����ᶼ���ڻ���� | |
| B�� | Fe��OH��3������ɫ�������ܲ������������ | |
| C�� | ���ۡ���ά�ء���Ȼ������Ȼ�߷��ӻ����� | |
| D�� | SiO2���ܺ�NaOH��Һ��Ӧ���ܺ�����ᷴӦ������������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2��HCl����������ͨ�뱥��Na2CO3��Һ�� | |
| B�� | Cl2��HCl����������ͨ�뱥��ʳ��ˮ�� | |
| C�� | NO2��NO����������ͨ��ˮ�� | |
| D�� | CO2��SO2����������ͨ�����ʯ��ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 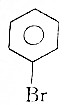 | B�� | 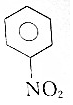 | C�� | C2H4 | D�� | C2H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ�� | B�� | ���� | C�� | ����� | D�� | Һ̬�Ȼ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com