
 ;B
;B
分析 (1)④植物油属于酯类物质,既能使溴水因发生化学变化褪色,也能使酸性高锰酸钾褪色的烃中有不饱和键,据此分析;
(2)烃不能与NaOH反应,酯能够在NaOH溶液中水解;
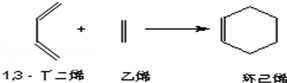
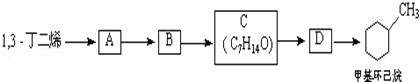
(3)根据碳原子数目可知,反应①为1,3-丁二烯与CH2=CH-CH3发生信息Ⅰ反应生成A,则A为 ,结合A发生信息Ⅱ中反应生成B,则B为
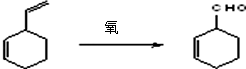
,结合A发生信息Ⅱ中反应生成B,则B为 ,结合C的分子式可知,B与氢气发生全加成反应生成C,C为
,结合C的分子式可知,B与氢气发生全加成反应生成C,C为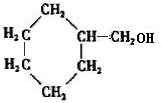 ,C发生消去反应生成D,D为
,C发生消去反应生成D,D为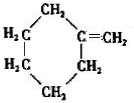 ,D发生加成反应生成甲基环己烷.
,D发生加成反应生成甲基环己烷.
解答 解:(1)植物油属于酯类物质,不是烃,甲苯和直馏汽油中没有能够使溴水因发生化学变化褪色的官能团,1,3-丁二烯中含有碳碳双键,能够与溴水发生加成反应,能够被酸性高锰酸钾氧化,故答案为:②;
(2)烃不能与NaOH反应,酯能够在NaOH溶液中水解,所以含有酯基的就能和NaOH反应,为④,
故答案为:④;
(3)(a)通过以上分析知,A的结构简式是 ,B的结构简式是
,B的结构简式是 ,
,
故答案为: ;
; ;
;
(b)据上述分析,加氢后产物与甲基环己烷互为同系物的是A,故答案为:A;
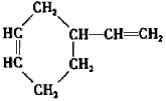
(c)A的结构简式是 ,其2个碳碳双键上的4个C原子都不等效,所以Br原子加成到4个C原子上的产物都不相同,其与HBr加成时的产物有4种,故答案为:4.
,其2个碳碳双键上的4个C原子都不等效,所以Br原子加成到4个C原子上的产物都不相同,其与HBr加成时的产物有4种,故答案为:4.
点评 本题考查有机物推断,侧重考查学生获取信息、加工信息、利用信息及分析推断能力,正确理解题给信息是解本题关键,题目难度中等,注意(3)题(c)中A发生加成反应产物种类判断,为易错点.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K、K2O、K2CO3、KHCO3 | B. | Na、Na2O2、NaOH、Na2CO3 | ||
| C. | K、K2O、KOH、K2CO3 | D. | Na、Na2O、NaOH、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用青霉素时,有些人可以不进行皮肤敏感试验 | |
| B. | 长期大量使用阿司匹林可预防疾病,没有副作用 | |
| C. | 对于标记“OTC”的药物,必需在医生指导下使用 | |
| D. | “是药三分毒”,必须按医嘱或药物说明书使用药物,防范药物不良反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

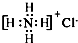
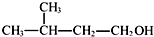
| A. | ①②③ | B. | ③④ | C. | ②④⑤ | D. | ①④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com