
分析 在盐酸溶液中,氢氧根全部由水电离出;而在氯化铁溶液中,氢离子和氢氧根全部来自于水的电离;在烧碱溶液中,氢离子全部来自于水的电离;在纯碱溶液中,氢离子和氢氧根全部来自于水的电离,然后根据由水电离出的氢离子和氢氧根的浓度相同来分析计算.
解答 25℃时,pH=3的盐酸和氯化铁溶液,c(H+)均为10-3mol/L,c(OH-)均为10-11mol/L.但盐酸溶液中,氢离子主要来自于酸的电离,氢氧根全部由水电离出,即由水电离出的c(OH-)=10-11mol/L,即水电离出的c(H+)也为10-11mol/L;而在氯化铁溶液中,氢离子和氢氧根全部来自于水的电离,而由于铁离子水解能结合氢氧根,故溶液中的氢离子是水电离出的全部氢离子,故在氯化铁溶液中,水电离出的c(H+)均为10-3mol/L.则pH=3的盐酸和氯化铁溶液中水电离出的氢离子浓度之比为10-11mol/L:10-3mol/L=1:108;
pH=10的烧碱溶液和纯碱溶液中c(H+)均为10-10mol/L,c(OH-)均为10-4mol/L.而在烧碱溶液中,氢离子全部来自于水的电离,故由水电离出的c(H+)为10-10mol/L,则水电离出的c(OH-)均为10-10mol/L;在纯碱溶液中,氢离子和氢氧根全部来自于水的电离,但由于碳酸根水解结合了氢离子,故溶液中的氢氧根全部来自于水的电离,即溶液中由水电离出的氢氧根的浓度c(OH-)为10-4mol/L,则水电离出的c(H+)为10-4mol/L,则pH=10的烧碱溶液和纯碱溶液中由水电离出的OH-浓度之比为10-10mol/L:10-4mol/L=1:106.
答:1:108;1:106.
点评 本题考查了在酸碱和能水解的盐溶液中由水电离出的氢离子和氢氧根浓度的有关计算,应注意到酸和碱对水的电离均有抑制作用,而盐的水解对水的电离有促进作用.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 可以用酒精灯直接加热锥形瓶和容量瓶 | |
| B. | 用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体 | |
| C. | 蒸馏时温度计水银球应高于蒸馏烧瓶支管口 | |
| D. | 振荡分液漏斗时应关闭其玻璃塞和活塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3是弱电解质 | B. | CO2是弱电解质 | ||
| C. | 酸X一定是共价化合物 | D. | 酸X一定是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①③④ | C. | ④⑤⑥ | D. | ①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
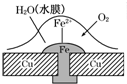 金属腐蚀是我们日常生活的常见现象.请根据如图回答下列问题:
金属腐蚀是我们日常生活的常见现象.请根据如图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2和NaOH | B. | NaCl和AgNO3 | C. | NaHCO3和HCl | D. | AlCl3和KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每摩尔物质约含有6.02×1023个粒子 | |
| B. | 摩尔是七个基本物理量之一 | |
| C. | 摩尔是物质的质量单位 | |
| D. | 摩尔是物质的数量单位 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com