
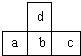
 如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )
如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )| A. | a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a | |
| B. | d的氢化物比b的氢化物稳定 | |
| C. | d与c不能形成化合物 | |
| D. | 原子半径的大小顺序是a>b>c>d |
分析 由元素在短周期中的位置可知d位于第二周期,a、b、c位于第三周期,a原子最外层电子数比次外层电子数少3个,故a原子最外层电子数为5,故a为P元素,可知b为S元素,c为Cl元素,d为O元素,结合元素周期律解答.
解答 解:由元素在短周期中的位置可知d位于第二周期,a、b、c位于第三周期,a原子最外层电子数比次外层电子数少3个,故a原子最外层电子数为5,故a为P元素,可知b为S元素,c为Cl元素,d为O元素.
A.同周期自左而右非金属性增强,故非金属性a<b<c,非金属性越强最高价氧化物对应水化物的酸性越强,故最高价氧化物对应水化物的酸性c>b>a,故A正确;
B.非金属性O>S,非金属性越强氢化物越稳定,故d的氢化物比b的氢化物稳定,故B正确;
C.氧元素与氯元素可以形成多种氯的氧化物,故C错误;
D.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径P>S>Cl>O,即a>b>c>d,故D正确;
故选C.
点评 本题考查结构位置性质关系应用,注意整体把握元素周期表的结构,熟练掌握元素周期律.


科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液:Na+、Fe3+、SO42-、Cl- | |
| B. | 饱和氯水:K+、Na+、Cl-、HSO3- | |
| C. | pH=13溶液:Na+、K+、SiO32-、Cl- | |
| D. | 1.0mol/L KNO3溶液:H+、Fe2+、Cl-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NO2气体受压缩后,颜色先变深后变浅 | |
| B. | 对2HI(g)?H2(g)+I2(g)平衡体系加压,颜色迅速变深 | |
| C. | 合成氨工业采用高温、高压工艺提高氨的产率 | |
| D. | 配制硫酸亚铁溶液时,常加入少量铁屑防止氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于30mL | B. | 等于30mL | C. | 大于20mL | D. | 等于20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 氯化铁和铜反应:Fe3++Cu═Fe2++Cu2+ | |
| C. | 石灰水与碳酸钠溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 鸡蛋壳在醋酸中溶解有气泡产生:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质为NaHCO3 | |
| B. | 溶质为Na2CO3 | |
| C. | 增重的4.4g为参加反应的CO2的质量 | |
| D. | 低温蒸干溶液,所得固体的质量为:(原溶液中NaOH的质量+4.4g) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com