
 2SO3(g) ��H��0�������о�Ŀ�ĺ�ͼʾ�������
2SO3(g) ��H��0�������о�Ŀ�ĺ�ͼʾ������� | ��� | A | B | C | D |
| Ŀ�� | ѹǿ��ƽ���Ӱ�� | �¶ȶ�ת���ʵ�Ӱ�� | ����O2Ũ�ȶ����ʵ�Ӱ�� | Ũ�ȶ�ƽ�ⳣ����Ӱ�� |
| ͼʾ | 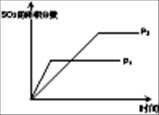 |  | 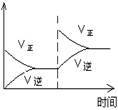 |  |


 ��������������������ϵ�д�
��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

 2SO3(g) ���÷�Ӧ��ƽ�ⳣ������ʽΪK= ��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ
2SO3(g) ���÷�Ӧ��ƽ�ⳣ������ʽΪK= ��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2BaO(s)+O2(g)�ﵽƽ�⡣�����¶Ȳ��䣬��С�����ݻ�����ϵ���´ﵽƽ�⣬����˵����ȷ����
2BaO(s)+O2(g)�ﵽƽ�⡣�����¶Ȳ��䣬��С�����ݻ�����ϵ���´ﵽƽ�⣬����˵����ȷ����| A��ƽ�ⳣ����С | B��BaO������ | C������ѹǿ���� | D��BaO2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Cr2O72- + H2O�� K��1��1014������0.05mol K2Cr2O7���Ƴ�1 L K2CrO4��Һ������c(Cr2O72��)��10��5mol/L����������Һ��pH
Cr2O72- + H2O�� K��1��1014������0.05mol K2Cr2O7���Ƴ�1 L K2CrO4��Һ������c(Cr2O72��)��10��5mol/L����������Һ��pH| A����7 | B����7 | C����7 | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
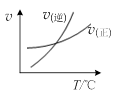
| A����ͼ�ױ�ʾ�ķ�Ӧ�������¶ȱ仯�Ĺ�ϵ��֪�÷�Ӧ�Ħ�H��0 |
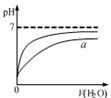
| B��ͼ�ұ�ʾpH��ͬ������������зֱ����ˮ����ҺpH�ı仯����������a��Ӧ���Ǵ��� |
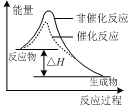
| C��ͼ����ʾ�÷�ӦΪ���ȷ�Ӧ���Ҵ����ܸı䷴Ӧ���ʱ� |
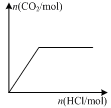
| D��ͼ����ʾ��Na2CO3��Һ����εμ�ϡ���ᣬ����CO2�������������ʵ����Ĺ�ϵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Fe��s����CO2��g����������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
Fe��s����CO2��g����������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���| T��K�� | 938 | 1100 |
| K | 0.68 | 0.40 |
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3��g�� ��H��0��2min��Ӧ�ﵽƽ�⣬����SO3Ϊ1.4mol,ͬʱ�ų�����Q kJ�������з�����ȷ����
2SO3��g�� ��H��0��2min��Ӧ�ﵽƽ�⣬����SO3Ϊ1.4mol,ͬʱ�ų�����Q kJ�������з�����ȷ����| A���ڸ������£���Ӧǰ���ѹǿ֮��Ϊ6��5.3 |
| B������Ӧ��ʼʱ�������Ϊ2L����v(SO3)��0.35mol/(L��min) |
| C�����ѡ����º�ѹ�¡���Ϊ����ѹ���������¡���Ӧ��ƽ���n(SO3)��1.4mol |
| D�����ѡ����º�ѹ�¡���Ϊ�����º����¡���Ӧ����ƽ��ʱ�ų���������Q kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ٺ�ɫ��ȥ��ԭ�������KMnO4��SCN-������ʹ[Fe��SCN��]2+��ʧ |
| B��[Fe��SCN��]2+��Fe3+��SCN-����λ����ϡ� |
| C���ں�ɫ��ȥ��ԭ����SO2����Ư���� |
| D��SCN-���ʵ������¿�ʧȥ���ӱ�����������Ϊ��SCN��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com