
【题目】酸性锌锰干电池和碱性锌锰干电池的构造简图如下所示,比较二者的异同,回答问题
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10﹣17 | 10﹣17 | 10﹣39 |
(1)酸性锌锰干电池的负极反应为
(2)碱性锌锰干电池在放电过程产生MnOOH,写出正极反应式
(3)维持电流强度为0.6A,电池工作10分钟,理论消耗Zng.(结果保留到小数点后两位,F=96500C/mol)
(4)用回收分离出的锌皮制作七水合硫酸锌,需去除少量杂质铁,除杂步骤如下:①加入足量稀硫酸和溶液将锌皮溶解,此时锌离子浓度为0.1mol/L
②调节溶液的pH为到之间(结果保留到小数点后一位),过滤除去含铁元素的沉淀.
【答案】
(1)Zn﹣2e﹣=Zn2+
(2)MnO2+e﹣+H2O=MnOOH+OH﹣ .
(3)0.12
(4)双氧水;2.7;6
【解析】解:(1)酸性锌锰干电池的负极为锌,负极反应为Zn﹣2e﹣=Zn2+ , 所以答案是:Zn﹣2e﹣=Zn2+;(2)在碱性锌锰原电池中,Zn易失电子作负极、二氧化锰作正极,正极上二氧化锰得电子发生还原反应,电极反应式为MnO2+e﹣+H2O=MnOOH+OH﹣ . 所以答案是:MnO2+e﹣+H2O=MnOOH+OH﹣;(3)持电流强度为0.6A,电池工作10分钟,则电量为0.6A×600s=360C,转移电子的物质的量为 ![]() =0.00373mol,则消耗Zn的质量为0.00373mol×
=0.00373mol,则消耗Zn的质量为0.00373mol× ![]() ×65g/mol=0.12g,所以答案是:0.12;(4)①根据表格中的信息可知,Fe(OH)3沉淀的生成更容易,而Zn(OH)2和Fe(OH)2的沉淀同时发生.故要想除去锌中的铁杂质,应将铁转化为Fe3+ , 而铁和稀硫酸只能反应为Fe2+ , 故应加入氧化剂,故可以加入绿色的氧化剂双氧水,所以答案是:双氧水;②由于调节pH的目的是使Fe3+沉淀完全而Zn2+不沉淀.而设Zn2+开始沉淀时所需的氢氧根的浓度为c(OH﹣),则有:0.1mol/L×c2(OH﹣)=10﹣17 , 解得c(OH﹣)=10﹣8mol/L,则c(H+)=10﹣6mol/L,pH=6.设Fe3+沉淀完全时所需的氢氧根的浓度为c(OH﹣),由于当一种离子沉淀完全时即浓度小于等于10﹣5mol/L时,则有:10﹣5mol/L×c3(OH﹣)=10﹣39 , 解得c(OH﹣)=
×65g/mol=0.12g,所以答案是:0.12;(4)①根据表格中的信息可知,Fe(OH)3沉淀的生成更容易,而Zn(OH)2和Fe(OH)2的沉淀同时发生.故要想除去锌中的铁杂质,应将铁转化为Fe3+ , 而铁和稀硫酸只能反应为Fe2+ , 故应加入氧化剂,故可以加入绿色的氧化剂双氧水,所以答案是:双氧水;②由于调节pH的目的是使Fe3+沉淀完全而Zn2+不沉淀.而设Zn2+开始沉淀时所需的氢氧根的浓度为c(OH﹣),则有:0.1mol/L×c2(OH﹣)=10﹣17 , 解得c(OH﹣)=10﹣8mol/L,则c(H+)=10﹣6mol/L,pH=6.设Fe3+沉淀完全时所需的氢氧根的浓度为c(OH﹣),由于当一种离子沉淀完全时即浓度小于等于10﹣5mol/L时,则有:10﹣5mol/L×c3(OH﹣)=10﹣39 , 解得c(OH﹣)= ![]() mol/L≈0.5×10﹣11mol/L,此时pH=2.7.故应调节pH在2.7到6之间.所以答案是:2.7;6.
mol/L≈0.5×10﹣11mol/L,此时pH=2.7.故应调节pH在2.7到6之间.所以答案是:2.7;6.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为________,反应④的化学方程式为____________________________________________________。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。反应②也在水溶液中进行,其离子方程式是_____________________________________ ,已知光照条件下D与F反应生成B,写出该反应的化学方程式:______________________________________
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷的结构式为________
(2)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是_________。
(3)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理下图所示,则通入a气体的电极名称为_____,通入b气体的电极反应式_______.(质子交换膜只允许H+通过)

(4)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如下图所示,则该反应的最佳温度应控制在_________左右。
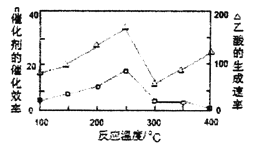
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为_________
(5)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. pH=1的溶液中:Fe2+、NO![]() 、SO
、SO![]() 、Na+
、Na+
B. 能使酚酞变红的溶液中:Na+、K+、NO![]() 、CO
、CO![]()
C. pH=13的无色溶液中:Cu2+、NO![]() 、HCO3-、Al3+
、HCO3-、Al3+
D. c(Fe3+)=0.1 molL-1的溶液中:K+、CO![]() 、I-、SCN-
、I-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 0.1 mol 的![]() 中,含有0.6NA个中子
中,含有0.6NA个中子
B. 7.1g Cl2通入足量的NaOH溶液中,反应转移电子的数目为0.2NA
C. 标准状况下,1.12L 的SO3所含的原子数目为0.2NA
D. 将足量的MnO2与含HCl 4 mol的浓盐酸混合后充分加热,生成的气体分子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的实验装置,丙为酚酞溶液润湿的淀粉碘化钾试纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1 , 一段时间后,A极产生的气体体积为44.8ml、B极产生的气体体积为22.4ml(都已换算成标况下的体积),回答下列问题: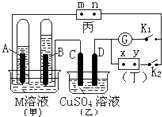
(1)M溶液可能是(填序号).
A.KCl溶液
B.Ba(OH)2溶液
C.KNO3溶液
D.CuCl2溶液
(2)乙池中盛有足量的硫酸铜溶液,D电极上的电极反应式为 , 此时向溶液中加入可以使溶液完全复原.
(3)滤纸丙上m点附近变为色,n点附近变为色,
(4)继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1 , 断开K2 , 发现电流计G指针发生偏转,若M为硫酸溶液,写出B电极上发生的反应式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( ) 
A.1 molH2中的化学键断裂时需要吸收436 kJ能量
B.2 molHCl分子中的化学键形成时要释放862 kJ能量
C.此反应的热化学方程式为:H2(g)+Cl2(g)═2HCl(g)△H=+183 kJ/mol
D.此反应的热化学方程式为: ![]() H2(g)+
H2(g)+ ![]() Cl2(g)═HCl(g)△H=﹣91.5 kJ/mol
Cl2(g)═HCl(g)△H=﹣91.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合物可用溶解、过滤、蒸发的操作达到分离目的的是( )
A. 硝酸钾与氯化钠的混合物
B. 石灰石与泥沙的混合物
C. 碘与酒精的混合物
D. 泥沙与氯化钠的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含碘元素。从海带中提取碘有如下步骤:①通入适量Cl2;②将海带灼烧成灰后加蒸馏水搅拌;③加CCl4振荡;④过滤。合理的操作顺序是( )
A.①②③④
B.②①③④
C.①③②④
D.②④①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com