
| A. | HClO的结构式:H-Cl-O | B. | 氨气分子的比例模型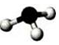 | ||
| C. | 原子核内有10个中子的氧原子:18O | D. | H2与H+互为同位素 |
分析 A、HClO中O原子分别与H原子和Cl形成共价键;
B、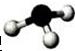 为球棍模型,不是比例模型;
为球棍模型,不是比例模型;
C.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.同位素为同种元素的不同原子之间的互称.
解答 解:A、HClO中O原子分别与H原子和Cl形成共价键,故HClO的结构式为H-O-Cl,故A错误;
B、 为氨气的球棍模型,氨气分子的比例模型为:
为氨气的球棍模型,氨气分子的比例模型为: ,故B错误;
,故B错误;
C.原子核内有10个中子的氧原子的质量数为18,该原子可以表示为:188O,故C正确;
D.同位素研究的是原子之间的关系,H2与H+之间不是原子,所以不属于同位素,故D错误;
关系C.
点评 本题考查了常见化学用语的判断,题目难度中等,涉及比例模型与球棍模型、结构式、元素符号、同位素等知识,注意掌握常见化学用语的概念及正确表示方法.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
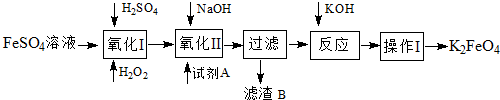
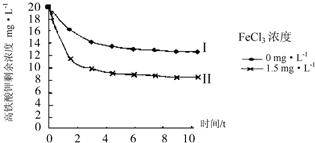
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元 素 | M | F | |
| 电离能 (kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在放电时,正极发生的反应是Pb+SO42-═PbSO4+2e- | |
| B. | 在放电时,该电池的负极材料是铅板 | |
| C. | 在充电时,电池中硫酸的浓度不断变小 | |
| D. | 在充电时,阳极发生的反应是PbSO4+2e-═Pb+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜是负极,铜片上有气泡产生 | B. | 电流从锌片经导线流向铜片 | ||
| C. | H+在铜片表面被还原 | D. | 铜片质量逐渐减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com