
| A. | 原子半径的大小顺序:r(W)>r(Y)>r(Z)>r(X) | |
| B. | 元素Z、W的简单离子的电子层结构相同 | |
| C. | 元素Y的简单气态氢化物的热稳定性比Z的强 | |
| D. | X、Y两种元素可形成分别含有10e-和18e-的化合物 |
分析 短周期主族元素X、Y、Z、W的原子序数依次增大,Z是地壳中含量最高的元素,则Z为O元素;由原子序数可知,Y处于第二周期,而X的原子半径比Y的小,则X只能处于第一周期,故X为H元素;X与W同主族,W原子序数大于氧,故W为Na;X与Y的最外层电子数之和等于Z的最外层电子数,则Y原子最外层电子数为6-1=5,故Y为N元素,据此解答.
解答 解:短周期主族元素X、Y、Z、W的原子序数依次增大,Z是地壳中含量最高的元素,则Z为O元素;由原子序数可知,Y处于第二周期,而X的原子半径比Y的小,则X只能处于第一周期,故X为H元素;X与W同主族,W原子序数大于氧,故W为Na;X与Y的最外层电子数之和等于Z的最外层电子数,则Y原子最外层电子数为6-1=5,故Y为N元素.
A.同周期自左而右原子半径减小、同主族自上而下原子半径增大,所有元素中H原子半径最小,故原子半径:r(Na)>r(N)>r(N)>r(O),故A正确;
B.元素Z、W的简单离子分别为O2-、Na+,离子核外均含有10个电子,离子的电子层结构相同,故B正确;
C.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性Y(N)<Z(O),所以Z的气态简单氢化物的热稳定性比Y的强,故C错误;
D.X、Y两种元素可形成NH3、N2H4,分子中分别含有10e-和18e-,故D正确,
故选C.
点评 本题考查原子结构和元素周期律,推断元素是解题关键,熟练掌握同一周期、同一主族元素性质递变规律,题目难度不大.


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:解答题
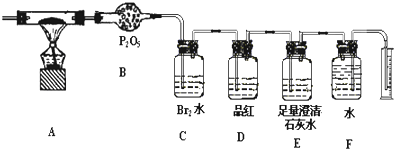
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液中:Al3+、Fe3+、SO42-、SCN- | |
| B. | 透明溶液中:MnO4-、K+、Na+、NO3- | |
| C. | FeCl3溶液中:Na+、K+、SO42-、I- | |
| D. | 强酸性溶液中:Na+、Fe2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
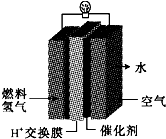 第29届奥运会期间,作为马拉松领跑车和电视拍摄车的汽车,
第29届奥运会期间,作为马拉松领跑车和电视拍摄车的汽车,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是常见原电池装置,电流表G发生偏转:
如图是常见原电池装置,电流表G发生偏转:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制Cu(OH)2悬浊液 | B. | KMnO4溶液 | C. | 溴水 | D. | FeCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com