
| A. | ①③⑤ | B. | ①②⑤ | C. | ①②③⑤ | D. | ①②③ |
分析 ①二氧化碳和碳酸钠反应生成碳酸氢钠,碳酸氢钠的溶解度小于碳酸钠的溶解度;
②依据胶体聚沉的性质及酸碱中和反应解答;
③硝酸根离子在酸性环境下能够氧化二氧化硫生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡沉淀;
④向石灰水中通入过量CO2,氢氧化钙与二氧化碳先反应生成碳酸钙沉淀,然后碳酸钙再与二氧化碳反应生成碳酸氢钙;
⑤硅酸钠与盐酸反应生成硅酸沉淀.
解答 解:①向饱和碳酸钠溶液中通入过量的CO2,碳酸钠和二氧化碳、水反应生成碳酸氢钠,反应为Na2CO3+CO2+H2O=2NaHCO3,碳酸氢钠的溶解性小于碳酸钠的溶解性,原碳酸钠溶液是饱和溶液,生成碳酸氢钠后溶液变成过饱和溶液,所以会析出部分碳酸氢钠晶体,所以不出现先产生沉淀,然后沉淀又溶解现象,故A选;
②向Fe(OH)3胶体中逐滴滴入硫酸,先发生聚沉生成氢氧化铁沉淀,氢氧化铁与硫酸发生酸碱中和反应,生成可溶性硫酸铁,所以现象为:先出现沉淀,然后沉淀溶解,故不选;
③硝酸根离子在酸性环境下能够氧化二氧化硫生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡沉淀,硫酸钡不溶于水,所以不会出现先产生沉淀,然后沉淀又溶解的现象,故选;
④向石灰水中通入过量CO2,氢氧化钙与二氧化碳先反应生成碳酸钙沉淀,然后碳酸钙再与二氧化碳反应生成碳酸氢钙,碳酸氢钙易溶于水,所以现象:先产生沉淀,然后沉淀又溶解,故不选;
⑤硅酸钠与盐酸反应生成硅酸沉淀,硅酸不溶液水,现象是出现沉淀,但是沉淀不溶解,故选;
故选:A.
点评 本题考查了元素化合物知识,熟悉物质的性质及发生的反应是解题关键,题目难度不大.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:多选题
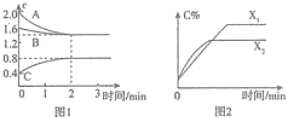
| A. | 0~2分钟、2~3分钟内用A浓度表示的平均反应速率:v(0~2)>v(2~3)>0 | |
| B. | 容器中发生的反应可表示为:3A(g)+B(g)?2C(g) | |
| C. | 若X表示温度,则生成C的反应是放热反应 | |
| D. | 若其他条件不变,仅减小起始时B的浓度,开始反应后C物质的浓度一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 铁在潮湿的空气中容易腐蚀 | |
| C. | 镀锌的铁制品比镀锡的铁制品耐用 | |
| D. | 常温下铝跟稀硫酸快速反应,跟浓硫酸不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
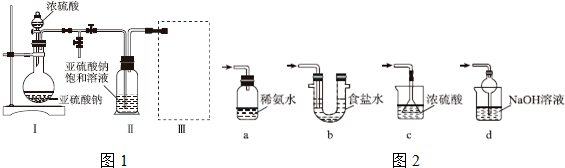

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池总反应的离子方程式为:Mg+H2O2+2H+═Mg2++2H2O | |
| B. | 负极的电极反应为:H2O2+2H++2e-═2H2O | |
| C. | 工作时,正极周围海水的pH减小 | |
| D. | 电池工作时,溶液中的H+向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
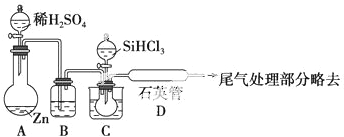
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
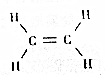
| A. | 乙烯是由碳、氢两种元素组成的 | |
| B. | 乙烯中碳元素的质量分数为85.7% | |
| C. | 乙烯是一种有机高分子化合物 | |
| D. | 乙烯中碳、氢两种元素的原子个数比是1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率:乙>甲 | B. | 平衡时O2的浓度:乙>甲 | ||
| C. | 平衡时SO2的转化率:乙>甲 | D. | 平衡时SO2的体积分数:乙>甲 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com