
����Ŀ���ܶ��ʻ���ˮ������ζ���������Ļ�����ͼ��ͼ1����ϩ��Ϊԭ����ȡ���������Ĺ��̣����ֲ���ͷ�Ӧ��������ȥ���� 
��ش��������⣺
��1��B�Ľṹ��ʽΪ ��
��2����ϩ��ˮ��Ӧ����A�ķ�Ӧ����Ϊ ��
��3��A��C��Ӧ�������������Ļ�ѧ����ʽΪ �� �䷴Ӧ����Ϊ ��
��4��ʵ���ҿ���ͼ2װ����ȡ���������� �����Թ�a�мӺ�����Լ�����Ҫ����2��3������Ƭ���������� ��
���Թ�b��ʢ�б���̼������Һ�����ɵ����������ڸ���Һ������ϡ����¡����㣬�÷�Һ�ķ���������ò�Ʒ�������Ҫ������ �� �Թ�b�еĵ��ܿ�Ӧ��Һ���Ϸ��������뵽Һ�����£���ԭ���� ��
���𰸡�
��1��CH3CHO
��2���ӳɷ�Ӧ
��3��CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O����������ȡ������Ӧ
CH3COOCH2CH3+H2O����������ȡ������Ӧ
��4����ֹ���У��ϣ���Һ©�����ձ��ȣ�����ֹ����
���������⣺��ͼ��֪����ϩ��ˮ�����ӳɷ�Ӧ����AΪCH3CH2OH��A��������������BΪCH3CHO��A��C��Ӧ��������������CΪCH3COOH����1��B�Ľṹ��ʽΪCH3CHO�����Դ��ǣ�CH3CHO�� ��2����ϩ��ˮ��Ӧ����A�ķ�Ӧ����Ϊ�ӳɷ�Ӧ�����Դ��ǣ��ӳɷ�Ӧ����3��A��C��Ӧ�������������Ļ�ѧ����ʽΪCH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O����Ӧ����Ϊ��������ȡ������Ӧ�����Դ��ǣ�CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O����Ӧ����Ϊ��������ȡ������Ӧ�����Դ��ǣ�CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O����������ȡ������Ӧ����4�������Թ�a�мӺ�����Լ�����Ҫ����2��3������Ƭ���������Ƿ�ֹ���У����Դ��ǣ���ֹ���У����Թ�b��ʢ�б���̼������Һ�����ɵ���������������ˮ���ܶȱ�ˮС�������������ڸ���Һ���ϲ㣬�÷�Һ�ķ���������ò�Ʒ�������Ҫ�����Ƿ�Һ©�����ձ��ȣ����Թ�b�еĵ��ܿ�Ӧ��Һ���Ϸ��������뵽Һ�����£���ԭ���Ƿ�ֹ���������Դ��ǣ��ϣ���Һ©�����ձ��ȣ�����ֹ������
CH3COOCH2CH3+H2O����������ȡ������Ӧ����4�������Թ�a�мӺ�����Լ�����Ҫ����2��3������Ƭ���������Ƿ�ֹ���У����Դ��ǣ���ֹ���У����Թ�b��ʢ�б���̼������Һ�����ɵ���������������ˮ���ܶȱ�ˮС�������������ڸ���Һ���ϲ㣬�÷�Һ�ķ���������ò�Ʒ�������Ҫ�����Ƿ�Һ©�����ձ��ȣ����Թ�b�еĵ��ܿ�Ӧ��Һ���Ϸ��������뵽Һ�����£���ԭ���Ƿ�ֹ���������Դ��ǣ��ϣ���Һ©�����ձ��ȣ�����ֹ������


 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������½�KOH��Һ�μӵ�������(H2X) ��Һ�У������Һ��pH������Ũ�ȱ仯�Ĺ�ϵ��ͼ��ʾ������������ȷ����
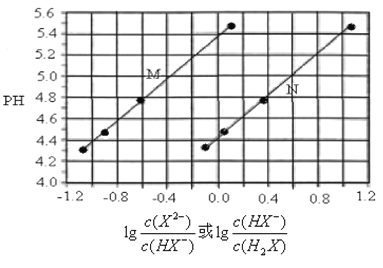
A. Ka2(H2X)��������Ϊ10�C4
B. KHX��Һ��c(H+)>c(OH-)
C. ����N��ʾpH��1g[c(X2-)/c(HX-)]�ı仯��ϵ
D. �������Һ������ʱ��c(K+) >c(HX-) > c(X2-) > c(OH-) =c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��������н��з�ӦA��g��2B��g��+C��g������A��Ũ����0.1molL��1����0.06molL��1��20s����ô��0.06molL��1����0.024molL��1 �� ��Ҫʱ������ǣ� ��
A.18s
B.12s
C.30s
D.10s
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪԪ�����ڱ���һ����,����X��Y��Z��WΪ���ֶ�����Ԫ�ء�ZԪ��ԭ�Ӻ���K����M���ϵĵ�������ȡ�����˵������ȷ����(����)
![]()
A. YԪ�ص�����������Ӧ��ˮ����Ļ�ѧʽΪH3YO4
B. Y�������̬�⻯���ˮ��Һ��������
C. ԭ�Ӱ뾶��С�����˳��ΪX<Z<Y<W
D. X��Z����Ԫ�ص���������������ѧ����������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ұ���������ѧ������������ǵ�ת����ϵ��ͼ��ʾ��ijЩ�����Ͳ��ֲ�������ȥ��������˵���������

A. ����Ϊһ��ǿ������ɫ��ӦΪ��ɫ����Ӧ�٢ڿ��ܶ�����������ԭ��Ӧ
B. �����£�����Ϊ��ɫ���壬��Ϊ����ɫ���壬��ס��ҿ�����ͭ��ϡ����
C. ����Ϊ���ȼ�ղ����Ϊˮ�����첻�����ڸ����
D. ����ΪŨ���ᣬ��ΪMnO2���������ʹƷ����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��ŵ������ѧ���ɷ�������������������λ��ѧ�һ�������������������ӻ����������ϳ��������Ĺ��ס����������ɷ��ӹ��������ڵ���ʵ���
A.H2SO4 B.NaCl C.NH3 D.Fe
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����14�֣�ij�����������̿���п����Ҫ�ɷ�ΪMnO2��ZnS�����������FeS��CuS��Al2O3�����ʣ�Ϊԭ����ȡZn��MnO2��
��1����һ�������£��������ֿ����������Һ������ã���ƽ���µĻ�ѧ����ʽ��
MnO2 + FeS + H2SO4![]() MnSO4 + Fe2(SO4)3 + S + H2O
MnSO4 + Fe2(SO4)3 + S + H2O
��2�������ú���Mn2+��Fe3+��Cu2+��Al3+��Zn2+��������Һ�����µĹ�ҵ���̽��в�����������Һ��IV���������Һ��IV������MnO2��Zn��
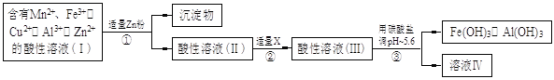
a���������м�Zn�ۺ�����Ӧ�����ӷ���ʽΪ ��
b���������м�������X��������ʲô ��X����ѡ��Ļ�ѧʽ�� ��
c��������������̼���εĻ�ѧʽ�� ��
��3��Ϊ�˴����������в�����Fe(OH)3��Al(OH)3����������л���Al(OH)3��������������µ��й�����ͼ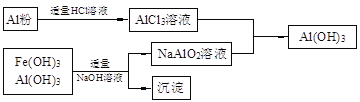
a��AlCl3��Һ��NaAlO2��Һ��Ӧ����AI(OH)3�����ӷ���ʽΪ �����ܹ��õ�n molAl(OH)3�������ĵ�NaOH��HCl����������mol���ֱ�Ϊ �� ��
b����ʹ���������̻��մ�������Ƚ�����������������������
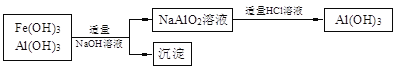
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������з�ɢϵ�����ȶ�����
A. ���� B. �Ȼ�����Һ C. ��ˮ D. ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A+��B����C2����D��E��F�ֱ��ʾ����18�����ӵļ����������ӻ���ӣ�����ش��������⣺
��1��AԪ����________��BԪ����________��CԪ����________����Ԫ�ط��ű�ʾ����
��2��D��������Ԫ����ɵ�˫ԭ�ӷ��ӣ��õ���ʽ��ʾ���γɹ���________��
��3��E�����к�18�����ӵ���������������ǿ�ķ��ӣ������ʽ��________������ˮ��Ӧ�Ļ�ѧ����ʽΪ________��
��4��F�����к���6��ԭ�ӣ��仯ѧʽ��________��________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com