
【题目】为探究不含结晶水的白色正盐X(仅含三种元素)的组成和性质,设计并完成如下实验:

已知:M(X)=270g·mol-1,灼烧X并透过蓝色钴玻璃片可看到紫色火焰。请回答:
(1)无色液体B的化学式是____。
(2)固体X加热分解的化学方程式是____。
(3)将X加入MnSO4溶液中,溶液变成紫红色,该反应的离子方程式为____。
【答案】SO3 2K2S2O8![]() 2K2SO4+2SO3↑+O2↑ 2Mn2++5S2O82-+8H2O=2MnO4-+10SO42-+16H+
2K2SO4+2SO3↑+O2↑ 2Mn2++5S2O82-+8H2O=2MnO4-+10SO42-+16H+
【解析】
不含结晶水的白色正盐X(仅含三种元素)5.40g,加热分解生成混合气体A和无色固体A,无色固体A加入盐酸和足量氯化钡溶液生成白色沉淀C为BaSO4,物质的量=![]() =0.02mol,说明A中含硫酸根离子,混合气体A冷却至室温得到气体B和无色液体B,加入盐酸和足量氯化钡溶液得到白色沉淀D为BaSO4,物质的量=
=0.02mol,说明A中含硫酸根离子,混合气体A冷却至室温得到气体B和无色液体B,加入盐酸和足量氯化钡溶液得到白色沉淀D为BaSO4,物质的量=![]() =0.02mol,说明无色液体B为SO3,气体B通过灼热氧化铜网,铜网变黑色增重0.32g,说明气体B为O2,增重的是生成氧气的质量,氧气物质的量=
=0.02mol,说明无色液体B为SO3,气体B通过灼热氧化铜网,铜网变黑色增重0.32g,说明气体B为O2,增重的是生成氧气的质量,氧气物质的量=![]() =0.01mol,混合气体A为SO3和O2的混合气体,已知:M(X)=270gmol-1,灼烧X并透过蓝色钴玻璃片可看到紫色火焰,证明X中含钾元素,利用元素守恒计算得到X的化学式,含n(S)=0.04mol,无色固体A为K2SO4,n(K)=0.04mol,混合气体A为SO3和O2的混合气体,则X中含氧元素物质的量n(O)=
=0.01mol,混合气体A为SO3和O2的混合气体,已知:M(X)=270gmol-1,灼烧X并透过蓝色钴玻璃片可看到紫色火焰,证明X中含钾元素,利用元素守恒计算得到X的化学式,含n(S)=0.04mol,无色固体A为K2SO4,n(K)=0.04mol,混合气体A为SO3和O2的混合气体,则X中含氧元素物质的量n(O)=![]() =0.16mol,n(K):n(S):(O)=0.04:0.04:0.16=1:1:4,结合元素物质的量和原子守恒得到反应生成物为2K2SO4+2SO3+O2,原子守恒得到反应物2K2S2O8,分解的化学方程式:2K2S2O8
=0.16mol,n(K):n(S):(O)=0.04:0.04:0.16=1:1:4,结合元素物质的量和原子守恒得到反应生成物为2K2SO4+2SO3+O2,原子守恒得到反应物2K2S2O8,分解的化学方程式:2K2S2O8![]() 2K2SO4+2SO3↑+O2↑,据此分析回答问题。
2K2SO4+2SO3↑+O2↑,据此分析回答问题。
(1)分析可知无色液体B的化学式是SO3;
(2)固体X加热分解的化学方程式是:2K2S2O8![]() 2K2SO4+2SO3↑+O2↑;
2K2SO4+2SO3↑+O2↑;
(3)将X加入MnSO4溶液中,溶液变成紫红色,说明锰离子被氧化为高锰酸钾,反应的离子方程式:2Mn2++5S2O82-+8H2O=2MnO4-+10SO42-+16H+。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】实验室制取、净化并收集氯气涉及以下几个主要阶段:
![]()
(1)写出实验室制取![]() 的离子方程式______________,
的离子方程式______________,![]() 表示阿伏伽德罗常数,若有
表示阿伏伽德罗常数,若有![]() 的
的![]() 被氧化,则转移的电子总数为______________;将足量的MnO2投入到含2mol HCl的浓盐酸中,充分加热,可生成Cl2______________(填>0.5mol;=0.5mol;<0.5mol)
被氧化,则转移的电子总数为______________;将足量的MnO2投入到含2mol HCl的浓盐酸中,充分加热,可生成Cl2______________(填>0.5mol;=0.5mol;<0.5mol)
(2)现有以下3种试剂:A.饱和食盐水B.浓硫酸C.![]() 溶液,请在以上试剂中选择并回答填空:Y溶液应选用___________ (填写序号):X试剂的作用_________。
溶液,请在以上试剂中选择并回答填空:Y溶液应选用___________ (填写序号):X试剂的作用_________。
(3)某兴趣小组的同学为探究和比较![]() 和氯水的漂白性,设计了如下的实验装置。
和氯水的漂白性,设计了如下的实验装置。

①实验室用装置![]() 制备
制备![]() 。某同学在实验时发现打开
。某同学在实验时发现打开![]() 的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:_______;
的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:_______;
②反应开始一段时间后,观察到![]() 、
、![]() 两试管中的品红溶液都出现褪色的现象,取下后两试管外观无区别,请你帮助设计实验加以鉴别,你的操作是____________。
两试管中的品红溶液都出现褪色的现象,取下后两试管外观无区别,请你帮助设计实验加以鉴别,你的操作是____________。
③若左右气体流速相同,写出C烧杯中的化学方程式____________。(写总方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目要求写出相应的化学方程式。
(1)乙二酸与乙二醇通过缩聚反应生成聚酯: ________。
(2)对苯二甲酸与乙二醇合成涤纶: ________________。
(3)苯酚与甲醛合成线状酚醛树脂: ___________。
(4)1,3-丁二烯合成顺丁橡胶: __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
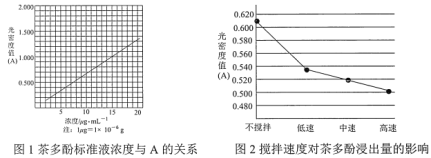
【题目】茶叶中的茶多酚是一种天然抗氧化剂(其抗氧化能力是VC的5~10倍),它易溶于水、乙醇、乙酸乙酯,难溶于氯仿。在酸性介质中,茶多酚能将Fe3+还原为Fe2+,Fe2+与![]() 生成的深蓝色配位化合物
生成的深蓝色配位化合物![]() 对特定波长光的吸收程度(用光密度值A表示)与茶多酚在一定浓度范围内成正比。A与茶多酚标准液浓度的关系如图1所示:
对特定波长光的吸收程度(用光密度值A表示)与茶多酚在一定浓度范围内成正比。A与茶多酚标准液浓度的关系如图1所示:
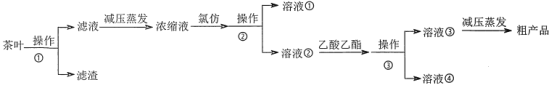
某实验小组设计如下实验流程从茶叶中提取茶多酚:
请回答下列问题:
(1)操作①用水浸取茶多酚时,实验小组发现搅拌速度对茶多酚浸出量的影响如图2所示,原因是____。若用乙醇浸取茶多酚操作如下:称取10g茶叶末,用滤纸包好,装入恒压滴液漏斗中,圆底烧瓶内加沸石和适量乙醇,如图3安装后,通冷凝水,加热套加热,当乙醇被加热沸腾后,控制加热套温度在90℃。为使恒压漏斗内液面高出茶叶包约0.5cm,并保持约1h,可行的操作方法是____。
(2)减压蒸发相对于一般蒸发的优点是____。氯仿的作用是____。
(3)下列有关实验基本操作不正确的是___。
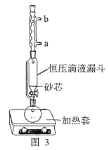
A. 图3中冷凝水流向为a进b出
B. 分液漏斗使用前须检验是否漏水并洗净备用
C. 操作①过滤时,可用玻璃棒适当搅拌以加快分离速度
D. 萃取过程中,经振摇并放气后,将分液漏斗置于铁圈上立即分液
(4)下列关于振摇操作的示意图,正确的是____。
A. 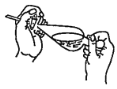 B.
B. 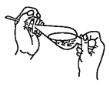 C.
C. 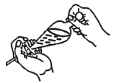 D.
D. 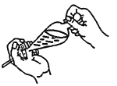
(5)称取1.25g粗产品,用蒸馏水溶解并定容至1000mL,移取该溶液1.00mL,加过量Fe3+和![]() 酸性溶液,用蒸馏水定容至100mL后,测得溶液光密度值A=0.800,则产品的纯度是____(以质量分数表示)。
酸性溶液,用蒸馏水定容至100mL后,测得溶液光密度值A=0.800,则产品的纯度是____(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所给信息或标志,判断下列说法错误的是()
A.在实验室和生产生活中,安全都是避免伤害和事故的保障—用肥皂液涂在天然气管道接口处检验是否漏气
B. 在运送硫酸的油罐车上贴有该标志
在运送硫酸的油罐车上贴有该标志
C. 看到有该标志的丢弃物,应远离并报警
看到有该标志的丢弃物,应远离并报警
D. 贴有该标志的物品是可回收物
贴有该标志的物品是可回收物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验合理的是
A.用![]() 悬浊液不能鉴别乙醇、乙醛、乙酸
悬浊液不能鉴别乙醇、乙醛、乙酸
B.焰色反应后,要用稀硫酸洗涤铂丝并在火焰上燃烧至无色
C.可用O2除去CO2中混有的CO
D.将溴水中的溴提取出来的方法是用CCl4少量多次进行萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F均为周期表中前四周期的元素,原子序数依次增大。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体可做半导体材料;F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为________
(2)B的氯化物的熔点比D的氯化物的熔点高的理由是____________。
(3)A的简单氢化物的中心原子采取______杂化,E的低价氧化物分子的空间构型是____。
(4)F的核外电子排布式是_____,A、F形成某种化合物的晶胞结构如图所示(其中A显-3价),则其化学式为_______。
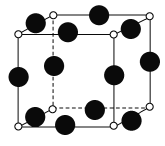
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.阅读、分析下列两个材料:
材料一
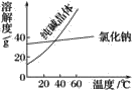
材料二
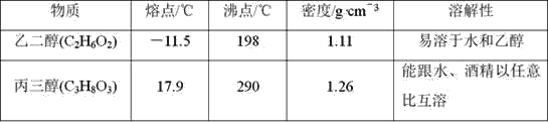
回答下列问题(填字母):
A.蒸馏法 B.萃取法C.“溶解、结晶、过滤”的方法 D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好选用________。
(2)将乙二醇和丙三醇相互分离的最佳方法是________。
Ⅱ.阅读下列材料,按要求回答问题。
酒精、苯、CCl4、煤油都是有机溶剂,有机溶剂之间大都能互溶;碘(I2)难溶于水,易溶于有机溶剂,其溶液呈紫色;溴(液溴)的性质与碘相似,其溶液呈橙色。
(1)下列能用分液漏斗进行分离的是________(填字母)。
A.液溴和CCl4B.酒精和煤油
C.CaCl2和Na2SO4D.苯和蒸馏水
(2)在酒精、苯、CCl4、NaCl、蒸馏水五种试剂中:
①能把碘单质从碘水中萃取出来的是________,进行分液之后________(填“能”或“不能”)得到纯净的碘单质。
②能把溴从溴水中萃取出来,并在分液时溴从分液漏斗下端流出的是________,若观察发现提取Br2以后的水还有颜色,解决该问题的方法是_________________________。
③CCl4能把碘酒中的碘萃取出来吗?________,为什么? ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是
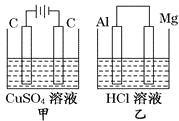
A. 溶液的质量变化:甲减小,乙增大
B. 溶液pH变化:甲减小,乙增大
C. 相同条件下产生气体的体积:V甲=V乙
D. 电极反应式:甲中阴极:Cu2++2e-==Cu,乙中负极:Mg-2e-==Mg2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com