
【题目】常温下0.1mol/L醋酸溶液的PH=a,下列能使溶液PH=(a+1)的措施是
A. 将溶液稀释到原体积的10倍
B. 加入适量的醋酸钠固体
C. 加入等体积0.2molL-1盐酸
D. 提高溶液的温度
科目:高中化学 来源: 题型:
【题目】下列混合物的分离或提纯操作不正确的是( )
A.除去N2中的少量O2,可通过灼热的Cu网后,收集气体
B.除去FeCl3溶液中Fe(OH)3沉淀可以过滤
C.除去乙醇中的少量NaCl,可用蒸馏的方法
D.重结晶不能用于提纯物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在澄清透明的强酸性溶液中能大量共存的是( )
A. NH4+、Fe3+、SO42-、NO3- B. K+、Na+、CO32-、NO3-
C. K+、NH4+、OH-、SO42- D. Na+、K+、AlO2-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组中的两对物质,都能用分液漏斗分离且有机物层由分液漏斗上口倒出的是( )
A.汽油和水、四氯化碳和水
B.汽油和水、食用油和水
C.食用油和水、醋酸和水
D.葡萄糖和水、酒精和水
查看答案和解析>>
科目:高中化学 来源: 题型:
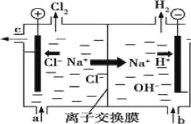
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。完成下列填空:
(1)写出电解饱和食盐水的离子方程式 。
(2)离子交换膜的作用为 : 、 。
(3)精制饱和食盐水从图 中________位置补充,氢氧化钠溶液从图中 位置流出。(选填“a”、“b”、“c”或“d”)
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 。
(5)室温下,0.1mol/LNaClO溶液的pH 0.1 mol/LNa2SO3溶液的pH。(选填“大于”、“小于”或“等于”)
(6)浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明溶液中,下列各组中的离子一定能大量共存的是:
A. K+、Fe2+、NO3-、H+ B. Na+、Pb2+、NO3-、SO42-
C. Na+、H+、Cl-、CO32- D. Na+、Ca2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和联氨(N2H4)既是一种工业原料,又是一种重要的工业产品。
(1)实验室可用氯化铵与消石灰反应制取氨气,其反应的化学方程式为 。
(2)联氨在一定条件下可按下式分解:3N2H4(g)=N2(g)+4NH3(g),已知断裂1molN—H、N—N及N≡N需吸收的能量依次为390.8kJ、193kJ、946kJ。若生成1molN2,则反应 (填“放出”或“吸收”) kJ的能量。
(3)NH3—O2燃料电池的结构如图所示。

①a极为电池的 (填“正”或“负”)极。
②当生成1molN2时,电路中流过电子的物质的量为 。
(4)联氨可以高效地脱除烟道气中的NO从而生成N2,该反应中氧化产物与还原产物的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“保护环境”是我国的基本国策。下列做法不应该提倡的是( )
A.采取低碳、节俭的生活方式
B.按照规定对生活废弃物进行分类放置
C.深入农村和社区宣传环保知识
D.经常使用一次性筷子、纸杯、塑料袋等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com